Catégories
nouveau blog
- Guide de sélection des électrolytes pour batteries : ce que les responsables des achats doivent savoir
- Équipement de laboratoire pour piles bouton : la liste de contrôle complète pour les laboratoires de R&D sur les batteries
- Comparaison des matériaux de cathode pour batteries : NMC, LFP et NCA
- Tendances de fabrication des batteries lithium-ion 2026 : Guide d’achat B2B
- Guide étape par étape du processus de fabrication des batteries lithium-ion
Tags
Matériaux cathodiques à très haute teneur en nickel LiNi0.91Co0.06Al0.03O2@Ca3(PO4)2
Mécanisme amélioré de stabilité au stockage du lithium des matériaux de cathode à très haute teneur en nickel LiNi0.91Co0.06Al0.03O2@Ca3(PO4)2
Auteur : ZHU Hezhen, WANG Xuanpeng, HAN Kang, YANG Chen, WAN Ruizhe, WU Liming, MAI Liqiang. Mécanisme de stabilité de stockage au lithium amélioré des matériaux de cathode à très haute teneur en nickel LiNi0.91Co0.06Al0.03O2@Ca3(PO4)2. Journal des matériaux inorganiques, 2022, 37(9): 1030-1036 DOI:10.15541/jim20210769
Le matériau à très haute teneur en nickel en tant que nouvelle cathode de batterie lithium-ion a attiré beaucoup d'attention en raison de sa capacité spécifique élevée, de sa haute tension et de son faible coût. Cependant, les microfissures générées, la pulvérisation mécanique et la transformation de phase irréversible pendant le cyclage entraînent une mauvaise stabilité du cyclage. Ici, une série de matériaux LiNi0.91Co0.06Al0.03O2 à ultra-haute teneur en nickel revêtus de Ca3(PO4)2 avec différentes épaisseurs (NCA@nCP) ont été préparés grâce à une stratégie de chimie humide facile. Parmi eux, NCA@1CP a manifesté une capacité de décharge spécifique de 204,8 mAh/g sous 2,7-4,3 V à 1C (1C=200 mA/g), avec un taux de rétention de capacité de 91,5 % après 100 cycles. Même après 300 cycles à 2C, la capacité de décharge spécifique a conservé 153,4 mAh/g. Les résultats de la caractérisation des matériaux confirment en outre que la coque de revêtement inhibe le mélange Li/Ni, transformation de phase irréversible et pulvérisation mécanique du NCA@1CP, améliorant considérablement la stabilité du cyclage. Ce travail montre que la stratégie de revêtement Ca3(PO4)2 a un grand potentiel d'application pour améliorer la stabilité au stockage du lithium des matériaux cathodiques à très haute teneur en nickel.
Afin de répondre à la demande de haute densité d'énergie des batteries lithium-ion, les chercheurs ont réalisé une série de progrès dans le domaine du développement de matériaux cathodiques à haute capacité spécifique réversible et haute tension de fonctionnement. Les matériaux de cathode en nickel à très haute teneur tels que LiNixM1-xO2 (M est un métal de transition, x≥0,9) présentent les avantages d'une capacité élevée, d'une haute tension et d'un faible coût, et constituent une direction de développement importante des matériaux de cathode pour le lithium à haute densité d'énergie. batteries ioniques à l'avenir. Kim a synthétisé le matériau à très haute teneur en nickel LiNi0.90Co0.05Mn0.05O2 par la méthode de co-précipitation, et la capacité spécifique de décharge initiale de la batterie Li-ion l'utilisant comme matériau de cathode était de 229,0 mAh/g. Le LiNi0.90Co0.09W0.01O2 synthétisé par Ryu présentait une capacité spécifique de décharge initiale ultra-élevée de 231,2 mAh/g. Cependant, le problème d'évanouissement de capacité limite l'application commerciale de ce type de matériaux, et un grand nombre d'études ont prouvé que les raisons peuvent être attribuées aux trois aspects suivants : (1) une teneur élevée en Ni aggravera le mélange Li/Ni, inhibera l'ion lithium diffusion et augmenter l'impédance de réaction, entraînant une perte de capacité réelle. (2) Le Ni4+ hautement actif formé dans les conditions d'élimination du lithium peut facilement avoir une réaction secondaire avec l'électrolyte et consommer l'électrode et l'électrolyte. Il favorise la transformation structurelle du matériau de la phase en couches à la phase spinelle désordonnée et à la phase de sel gemme et endommage gravement la structure cristalline du matériau, réduisant la stabilité du cycle.
La modification du revêtement est largement utilisée pour résoudre le problème de décoloration de la capacité des matériaux de cathode à haute teneur en nickel et améliorer la stabilité du cycle, parmi lesquels les matériaux d'oxyde sont les plus courants, tels que Al2O3, TiO2, SiO2 et ZrO2. Comparés aux oxydes, les phosphates ont une meilleure mobilité des ions lithium et une meilleure stabilité chimique, et ont fait l'objet d'une attention particulière dans le domaine de la modification de surface des matériaux de cathode à haute teneur en nickel ces dernières années. Xiao (XIAO YH, MIARA LJ, WANG Y, et al.) a confirmé par criblage informatique que le phosphate en tant que matériau de revêtement cathodique peut améliorer considérablement la stabilité. Les agents de revêtement de phosphate courants sont Mn3(PO4)2, BPO4, AlPO4 et Li3PO4. Yan (YAN PF, ZHENG JM, LIU J, et al.) a utilisé la technologie de dépôt de couche atomique pour enduire Li3PO4 sur la surface du matériau de cathode à haute teneur en nickel LiNi0.76Mn0.14Co0.10O2, qui supprime la transition de phase irréversible du matériau et améliore la cinétique de l'interface cathode-électrolyte. Feng (FENG Z, RAJAGOPALAN R, SUN D, et al.) a enduit Li3PO4-AlPO4-Al (PO3) 3 sur le matériau LiNi0.8Co0.1Mn0.1O2, et les performances du cycle ont été considérablement améliorées. Parmi les matériaux phosphatés, Ca3(PO4)2(CP) a une excellente stabilité chimique et thermique en raison de la forte liaison entre Ca2+ et [PO4]3-. Cependant, les matériaux de cathode à ultra-haute teneur en nickel modifiés par le revêtement CP n'ont pas encore été signalés. Par conséquent, une série de matériaux de cathode à très haute teneur en nickel LiNi0.91Co0.06Al0.03O2 revêtus de CP (NCA@nCP, n = 0,5, 1, 3) ont été préparés par une simple méthode chimique par voie humide. La structure, la morphologie et le mécanisme d'amélioration des performances électrochimiques de NCA@nCP ont été étudiés et analysés en détail.
Préparation du matériau cathodique
Ni0.91Co0.06Al0.03(OH)2 et LiOH·H2O ont été mélangés à un rapport molaire de 1:1,05, puis chauffés à 500 °C pendant 5 h à une vitesse de 5 °C/min dans une atmosphère d'oxygène, et puis chauffée à 720 °C pour l'isolation Après 15 h, et enfin refroidie naturellement à température ambiante, de la poudre de NCA noire a été obtenue. Peser 0,74 g de NH4H2PO4 et 2,28 g de Ca(NO3)2·4H2O et les dissoudre dans 100,0 mL d'eau et 100,0 mL d'éthanol anhydre, respectivement. Tout d'abord, 0,5 ml de solution de Ca(NO3)2 (solution A) et 0,5 ml de solution de NH4H2PO4 (solution B) ont été ajoutés à 50,0 ml d'éthanol absolu, puis 1,00 g de poudre de NCA ont été lentement ajoutés et enfin le solvant a été éliminé. par agitation et évaporation à 80 °C pour obtenir une poudre. Ensuite, la poudre a été frittée dans une atmosphère d'oxygène à 550 °C (vitesse de chauffage de 5 °C/min) pendant 2 h. A cette époque, la fraction massique de CP était de 0,5%, et le produit obtenu a été défini comme NCA@0.5CP. Lorsque chacune des solutions A et B est de 1,0 mL, la fraction massique de CP est de 1,0 % et le produit obtenu est défini comme NCA@1CP ; lorsque les solutions A et B sont chacune de 3,0 mL, la fraction massique de CP est de 3,0 % et le produit obtenu est défini comme NCA@3CP.
Caractérisation des matériaux
La structure cristalline du matériau a été caractérisée par diffraction des rayons X (diffraction des rayons X, XRD, D8 Discover X, rayonnement CuKα). Les données XRD raffinées ont été calculées par le logiciel GSAS en utilisant la méthode de Rietveld. La morphologie et la microstructure des matériaux ont été caractérisées par microscopie électronique à balayage (SEM, JEOL JSM-7100F) et microscopie électronique à transmission (TEM, JEM-2100F). La distribution des éléments du matériau a été observée par spectromètre à dispersion d'énergie des rayons X (spectromètre à dispersion d'énergie, EDS, EDX-GENESIS 60S). La spectroscopie photoélectronique à rayons X (spectroscopie photoélectronique à rayons X, XPS, VG MultiLab 2000) a été utilisée pour analyser la composition et la valence des éléments à la surface du matériau.
Essais électrochimiques
Le matériau de cathode actif, Super-P, et le fluorure de polyvinylidène ont été mélangés dans un rapport massique de 8:1:1, dispersés dans de la N-méthyl-2-pyrrolidone (NMP) et agités magnétiquement pendant 12 h, une suspension uniforme s'est formée , enduit sur une feuille d'aluminium, et enfin séché dans une étuve à vide à 120 ° C pendant 12 h pour éliminer la NMP. Coupez la feuille d'aluminium en une feuille d'électrode positive d'un diamètre de 10 mm, et la charge de masse de la feuille d'électrode positive coupée est de 2 à 3 mg/cm2. Des feuilles de lithium métallique (ou graphite) et des membranes poreuses en polypropylène (Celgard 2500) ont été utilisées comme contre-électrode et séparateur pour les demi-cellules (ou cellules complètes), respectivement. Les électrolytes utilisés dans la demi-cellule et la cellule complète sont des solutions de LiPF6 à 1 mol/L dissoutes dans du carbonate d'éthylène/carbonate de méthyle éthyle/carbonate de diéthyle (rapport volumique 1:1:1). Assemblez les piles bouton CR2016 dans une boîte à gants argon. Des expériences de charge/décharge électrochimique ont été réalisées à des intervalles de 2,7-4,3 V et 2,7-4,5 V à l'aide d'un système de test de batterie. utilisant un poste de travail électrochimique pour tester la voltamétrie cyclique (CV) à 0,1 mV/s et 2,7-4,3 V.
résultats et discussion
La figure 1(a) montre les schémas XRD des matériaux NCA et NCA@nCP. Les modèles XRD de tous les matériaux montrent des positions de pic et des formes de pic similaires, et aucun autre pic d'impureté. De plus, les pics de diffraction (006)/(102) et (108)/(110) du matériau après revêtement et avant revêtement étaient manifestement divisés, indiquant que le revêtement CP n'a pas modifié la structure en couches d'origine du matériau NCA. Dans de tels matériaux à base de nickel, puisque le rayon ionique (0,069 nm) de Ni2+ est similaire à celui de Li+ (0,076 nm), il est facile de migrer vers la couche de lithium, ce qui entraîne l'arrangement mixte de Li/Ni, et le rapport de I(003)/I(104) peut être Révéler le phénomène de mélange Li/Ni du matériau. Les résultats montrent que lorsque I(003)/I(104) est supérieur à 1,2, le matériau à base de nickel est généralement considéré comme ayant une structure en couches bien ordonnée, et plus I(003)/I(104) est grand, plus le degré de mélange Li/Ni est petit. Comme le montre le tableau S1, les I(003)/I(104) des matériaux NCA et NCA@nCP sont supérieurs à 1,2, dont NCA@1CP est le plus élevé (2,261), qui est supérieur à NCA (1,426), indiquant que le revêtement CP inhibe le Li du NCA. /Ni arrangement mixte. La figure 1(b) et la figure S1 sont les résultats XRD affinés de NCA@1CP et NCA et NCP@nCP, respectivement. Tous les pics de diffraction appartiennent à la structure en couches hexagonale de type O3. La différence de paramètres de réseau entre NCA et NCA@nCP est faible, ce qui indique que le CP n'entre pas dans le réseau du matériau NCA (tableau S2), les facteurs d'erreur (Rp et Rwp) du raffinement sont faibles et la fiabilité d'ajustement est haut. le I(003)/I(104) des matériaux NCA et NCA@nCP est supérieur à 1,2, dont NCA@1CP est le plus élevé (2,261), ce qui est supérieur à NCA (1,426), indiquant que le revêtement CP inhibe le Li de NCA. /Ni arrangement mixte. La figure 1(b) et la figure S1 sont les résultats XRD affinés de NCA@1CP et NCA et NCP@nCP, respectivement. Tous les pics de diffraction appartiennent à la structure en couches hexagonale de type O3. La différence de paramètres de réseau entre NCA et NCA@nCP est faible, ce qui indique que le CP n'entre pas dans le réseau du matériau NCA (tableau S2), les facteurs d'erreur (Rp et Rwp) du raffinement sont faibles et la fiabilité d'ajustement est haut. le I(003)/I(104) des matériaux NCA et NCA@nCP est supérieur à 1,2, dont NCA@1CP est le plus élevé (2,261), ce qui est supérieur à NCA (1,426), indiquant que le revêtement CP inhibe le Li de NCA. /Ni arrangement mixte. La figure 1(b) et la figure S1 sont les résultats XRD raffinés de NCA@1CP et NCA et NCP@nCP, respectivement. Tous les pics de diffraction appartiennent à la structure en couches hexagonale de type O3. La différence de paramètres de réseau entre NCA et NCA@nCP est faible, ce qui indique que le CP n'entre pas dans le réseau du matériau NCA (tableau S2), les facteurs d'erreur (Rp et Rwp) du raffinement sont faibles et la fiabilité d'ajustement est haut. La figure 1(b) et la figure S1 sont les résultats XRD affinés de NCA@1CP et NCA et NCP@nCP, respectivement. Tous les pics de diffraction appartiennent à la structure en couches hexagonale de type O3. La différence de paramètres de réseau entre NCA et NCA@nCP est faible, ce qui indique que le CP n'entre pas dans le réseau du matériau NCA (tableau S2), les facteurs d'erreur (Rp et Rwp) du raffinement sont faibles et la fiabilité d'ajustement est haut. La figure 1(b) et la figure S1 sont les résultats XRD affinés de NCA@1CP et NCA et NCP@nCP, respectivement. Tous les pics de diffraction appartiennent à la structure en couches hexagonale de type O3. La différence de paramètres de réseau entre NCA et NCA@nCP est faible, ce qui indique que le CP n'entre pas dans le réseau du matériau NCA (tableau S2), les facteurs d'erreur (Rp et Rwp) du raffinement sont faibles et la fiabilité d'ajustement est haut.
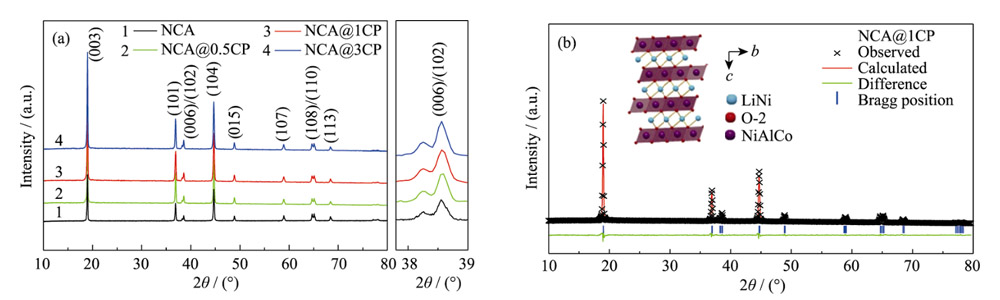
Fig. 1 (a) Modèles XRD de NCA et NCA@nCP (n = 0 , 5, 1, 3), et (b) Résultats de raffinement de Rietveld de NCA@1CP
La figure 2 (a) et la figure S2 sont les résultats de caractérisation SEM des matériaux NCA @ 1CP et NCA et NCP @ nCP, respectivement. La morphologie de tous les matériaux est sphérique et la morphologie sphérique des matériaux ne change pas après le revêtement CP. Les résultats de la caractérisation TEM montrent que le matériau NCA présente une bonne cristallinité avec un espacement des franges de réseau de 0, 47 nm, ce qui correspond au plan cristallin (003) du NCA (Fig. 2 (b)). En revanche, une couche de revêtement amorphe d'une épaisseur d'environ 5 nm a été clairement observée à la surface du matériau NCA @ 1CP (Fig. 2 (c)), indiquant que le CP était effectivement enduit à la surface du matériau NCA. La distribution des éléments des matériaux NCA @ 1CP et NCA a été analysée par EDS (Figure 2 (d) et Figure S3),

Fig. 2 (a) Image SEM de NCA@1CP, images TEM haute résolution de (b) NCA et (c) NCA@1CP, et (d) Cartographies élémentaires EDS de NCA@1CP
La composition et l'état de valence des éléments à la surface des matériaux ont été déterminés par analyse XPS des matériaux NCA et NCA@1CP. Comme le montre la figure 3 (a), quatre éléments de Ni, Co, Al et O sont détectés dans NCA, tandis qu'en plus des quatre éléments ci-dessus, des éléments Ca et P sont également détectés dans NCA @ 1CP, ce qui prouve que CP est enduit avec succès sur la surface du matériau NCA. Comme le montre la figure 3 (b), les deux pics à 856,5 et 873,3 eV appartiennent respectivement à Ni2p3/2 et Ni2p1/2. Le pic Ni2p3/2 peut en outre être ajusté à deux sous-pics à 854,7 et 855,8 eV, correspondant respectivement au Ni bivalent et trivalent. La surface du pic de Ni divalent dans le matériau NCA@1CP est plus petite que celle du matériau NCA, ce qui indique que la modification du revêtement CP réduit la teneur en Ni divalent dans le NCA et, dans une certaine mesure, peut inhiber le mélange Li/Ni. Les deux pics à 795,5 et 779,9 eV appartiennent respectivement à Co2p1/2 et Co2p3/2, ce qui indique que Co est trivalent (Figure 3(c)), tandis que le pic Al2p3/2 à 73,1 eV correspond bien au pic Al trivalent ( Figure 3(d)). De plus, les pics à 133,4 eV correspondant à P2p (Figure 3(e)) et 347,0 et 350,6 eV correspondant à Ca2p3/2 et Ca2p1/2 (Figure 3(f)) ont été détectés sur la surface du matériau NCA@1CP, tandis que aucun pic de P et Ca n'a été détecté dans le matériau NCA.
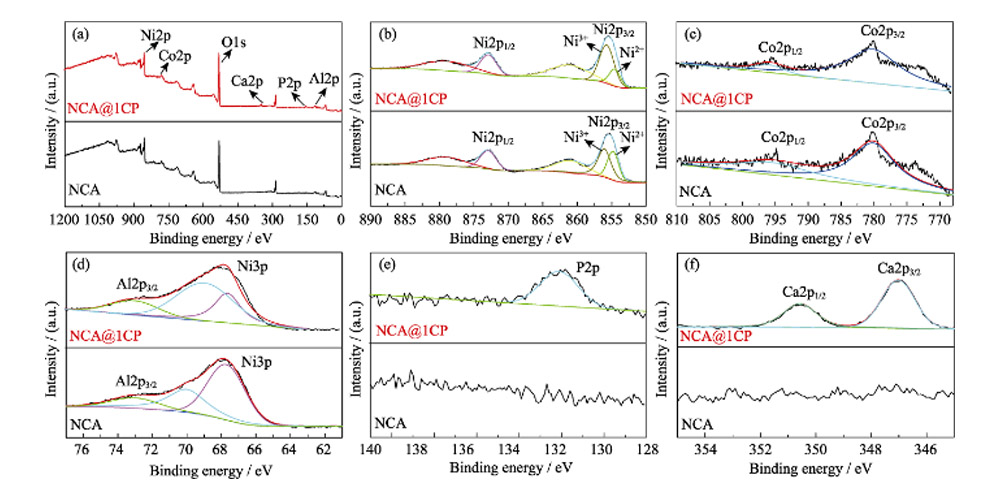
Fig. 3 (a) Relevé complet, (b) Ni2p, (c) Co2p, (d) Al2p, (e) P2p et (f) Spectres XPS Ca2p pour NCA et NCA@1CP
Dans la figure 4 (a, b) et la figure S4, les courbes CV des trois premiers tours de la demi-cellule lithium-ion assemblée avec des matériaux NCA et NCA @ nCP comme électrodes positives montrent qu'il existe trois paires de pics REDOX différents dans le test intervalle de 2,7-4,3V, correspondant à différents processus de transition de phase : Dans le processus d'extraction Li+, le pic d'oxydation à 3,83V représente la transition de la phase hexagonale à la phase monoclinique (H1-M), et les pics d'oxydation à 4,01 et 4,20 V représente la transition de la phase monoclinique à la phase hexagonale (M-H2) et la transition de la phase hexagonale à la phase hexagonale (H2-H3), respectivement. Les pics de réduction du processus d'incorporation de Li+ sont respectivement de 3,64 V, 3,96 V et 4,15 V. La différence de potentiel entre le pic d'oxydation et le pic de réduction au cours du cycle peut refléter la cinétique électrochimique du matériau. La différence de potentiel du pic REDOX initial de NCA est de 0,185 V, ce qui est supérieur à celui de NCA@0,5CP(0,154 V), NCA@1CP(0,112 V) et NCA@3CP(0,143 V) après revêtement. La polarisation du matériau NCA @ 1CP est la plus faible lors de l'incalation/élimination du lithium électrochimique. FIGUE. 4 (c) montre les courbes de charge et de décharge initiales d'une demi-cellule lithium-ion assemblée avec du matériau NCA et NCA@nCP comme électrode positive à 0,2 C (1 C = 200 mA/g) et 2,7-4,3 V. La capacité de décharge initiale de NCA est de 212,4 mAh/g, tandis que celle de NCA@nCP(n=0,5, 1, 3) est de 211,1, 210,4 et 203,3 mAh/g, respectivement. La figure 4(d) montre les performances du cycle de demi-cellule du matériau NCA et NCA@nCP à 1C et 2,7-4,3V. Afin de rendre le matériau d'électrode entièrement activé, la batterie a d'abord été chargée et déchargée à 0,2 C pendant 2 cycles, NCA@1CP à une capacité spécifique de décharge de 1 C de 204,8 mAh/g, 100 cycles après 187,5 mAh/g, la rétention de capacité correspondante le taux est de 91,5 %. Cependant, la capacité spécifique du NCA est de 203,2 mAh/g à 1C et de seulement 168,0 mAh/g après 100 cycles (le taux de rétention de capacité est de 82,6 %). Les résultats ci-dessus indiquent que le matériau NCA@1CP présente une excellente stabilité de cyclage aux tensions de coupure basses et hautes. La figure 4(f) montre les performances de cycle long du matériau NCA et NCA@1CP à 2C et 2,7-4,3V. La capacité de décharge initiale de NCA@1CP est de 184,9 mAh/g et 153,4 mAh/g restent après 300 cycles, soit 82,9 % de la valeur initiale. Cependant, la capacité spécifique de décharge initiale de NCA à 2C est de 173,5 mAh/g, et seulement de 115. 3 mAh/g après 300 cycles, soit seulement 66,4 % de la valeur initiale. La figure S5 (a ~ c) montre les performances de taux des matériaux NCA et NCA @ nCP dans la plage de 2,7 ~ 4,3 V. Les performances de débit de NCA sont médiocres, en particulier la capacité spécifique de 105,1 mAh/g à un débit ultra-élevé de 10C. En revanche, NCA@1CP a une capacité spécifique de décharge allant jusqu'à 130,4 mAh/g à 10C, montrant d'excellentes performances de débit.
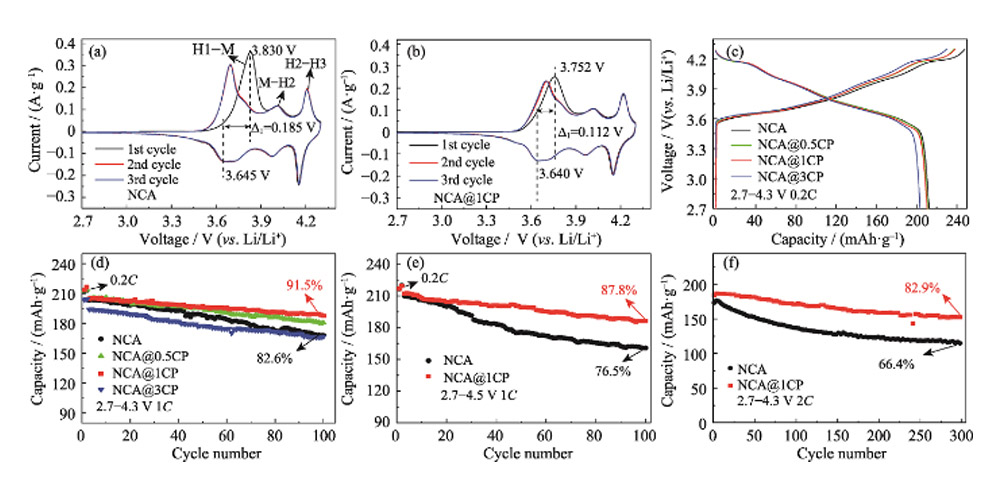
Fig. 4 Courbes CV pour (a) NCA et (b) NCA@1CP ; ( c ) courbes de charge-décharge initiales sous 2, 7-4, 3 V à 0, 2 C et ( d ) propriétés de cyclage sous 2, 7-4, 3 V à 1 C pour NCA et NCA @ nCP; Propriétés de cyclage pour NCA et NCA@1CP (e) sous 2,7-4,5 V à 1C et (f) sous 2,7-4,3 V à 2C
L'évolution de la structure cristalline des matériaux NCA et NCA @ 1CP au cours du cycle de charge-décharge a été suivie en temps réel par XRD in situ (Fig. 5). Comme le montre la figure 5 (a, b), au cours du premier cycle de charge à 4, 1 V, le cristal passe de la phase H1 à la phase H2, le pic de diffraction (003) se décale vers un angle faible et le paramètre de réseau c progressivement augmente. Ce phénomène peut être attribué à l'extraction des ions lithium du réseau, à la répulsion électrostatique accrue entre les couches de métal de transition et au plus grand espacement entre les couches. Après une charge supplémentaire, le cristal passe de la phase H2 à la phase H3, ce qui entraîne un déplacement brutal du pic de diffraction (003) vers un angle élevé et une contraction brutale du paramètre de réseau c. Cela peut être attribué à : (1) La nature covalente de la liaison Ni4+-O2- dans la couche de métal de transition est améliorée, la répulsion électrostatique entre les couches de métal de transition est affaiblie et l'espacement entre les couches est nettement plus petit. (2) L'extraction continue des ions lithium entre les couches de métal de transition affaiblit l'effet de support et réduit l'espacement intercouche. Le décalage angulaire maximal du pic de diffraction (003) du matériau NCA pendant la transition de phase H2-H3 est de 0,76 ° (Fig. 5 (e)). Bien que le matériau NCA @ 1CP présente également le processus de transition de phase H2-H3 (Fig. 5 (c, d)). Cependant, le décalage angulaire maximum du pic de diffraction (003) n'est que de 0,57° (Fig. 5(f)). La figure 5(g) montre les courbes d'évolution du paramètre de réseau c lors de la délithiation des matériaux NCA et NCA@1CP. Le rétrécissement du paramètre de réseau c de NCA@1CP (3. 5 %) est inférieur à celui de la NCA (4,1 %). Il est révélé que NCA@1CP a une meilleure stabilité structurelle. Les résultats XRD in situ montrent que le revêtement CP peut supprimer la transition de phase irréversible H2-H3 du matériau NCA, améliorant ainsi les performances électrochimiques du matériau.
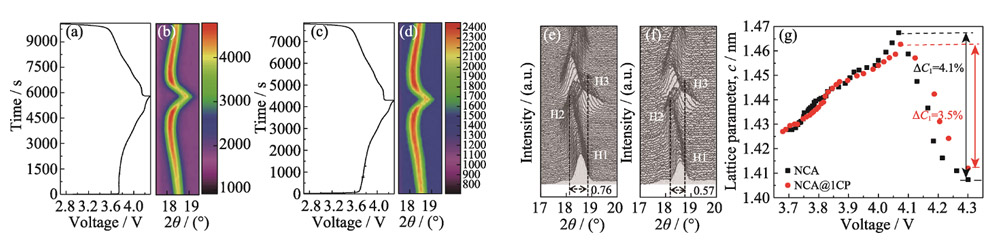
Fig. 5 Courbes de variation tension-temps pendant XRD in situ pour (a) NCA et (c) NCA@1CP ; Modèles XRD in situ pour (b, e) NCA et (d, f) NCA@1CP ; (g) Courbes de variation du paramètre de réseau c pendant la charge pour NCA et NCA@1CP
Afin d'évaluer de manière exhaustive l'effet du revêtement CP sur la morphologie et la microstructure des matériaux au cours du processus électrochimique, les pièces polaires des demi-cellules NCA et NCA@1CP après 100 cycles de charge-décharge (1C, 2,7 ~ 4,3 V) ont été caractérisées . Les résultats de la caractérisation SEM ont montré que seules quelques microfissures sont apparues à la surface du matériau NCA @ 1CP, tandis qu'un grand nombre de fissures sont apparues à la surface du matériau NCA et que certaines particules ont été pulvérisées (Fig. S6 (a, b) ). Il montre que la couche de revêtement CP inhibe dans une certaine mesure les microfissures de surface et le poudrage mécanique du matériau. La figure S6 (c – f) montre les modèles XRD des matériaux NCA et NCA @ 1CP avant et après 100 cycles. Les pics de diffraction (006) et (102) du NCA se chevauchent après 100 cycles (Fig. S6(d)), tandis que les pics de diffraction (006) et (102) de NCA @ 1CP sont toujours divisés après 100 cycles (Fig. S6 (f)) ). Cela montre que la couche de revêtement CP peut améliorer la stabilité de la structure NCA. Pour vérifier davantage la stabilité au stockage du lithium de NCA @ 1CP, une batterie complète de type pièce de monnaie a été assemblée avec des matériaux NCA et NCA @ 1CP comme électrode positive et du graphite comme électrode négative, respectivement (Fig. 6). À 1C (1C=200 mA/g) et 2,7~4,25 V, la capacité spécifique de décharge initiale de la cellule complète NCA@1CP est de 201,4 mAh/g. Après 70 cycles, la capacité spécifique de décharge s'est maintenue à 84,6 % de la valeur initiale (Fig. 6 (a)). Cependant, la capacité spécifique de décharge initiale de la cellule pleine NCA est de 198,6 mAh/g, et la capacité spécifique de décharge après 70 cycles n'est que de 65,6 % de la valeur initiale.
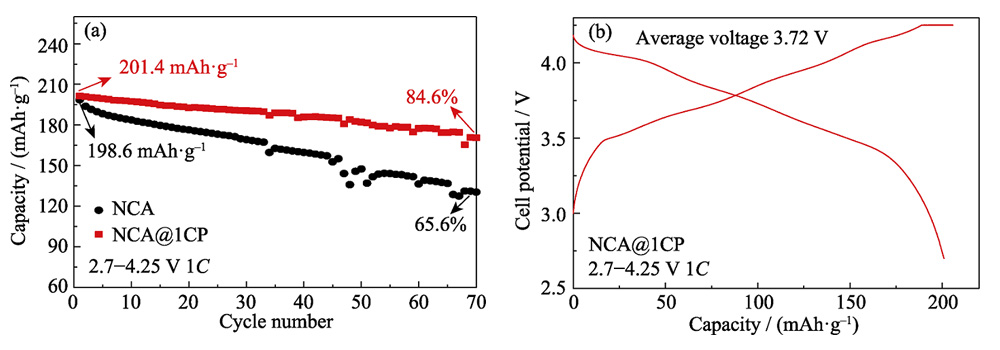
Fig. 6 (a) Propriétés de cyclage des cellules pleines à la fois NCA et NCA @ 1CP comme cathode, graphite comme anode sous 2,7-4,25 V à 1C, et (b) courbes de charge-décharge du deuxième cycle pour NCA @ 1CP en cellule pleine
Conclusion
Dans cette étude, les matériaux de cathode NCA @ 1CP ont été préparés par une stratégie chimique humide facile, ce qui a considérablement amélioré la stabilité au stockage électrochimique du lithium des matériaux NCA. Le matériau NCA@1CP présente un taux de rétention de capacité de 91,5 % après 100 cycles à 1C, montrant une durée de vie ultra-longue de plus de 300 cycles même à un taux élevé de 2C.
Le revêtement CP prolonge considérablement la durée de vie des matériaux cathodiques NCA, principalement en raison des aspects suivants :
(1) L'introduction de la couche de revêtement CP réduit le degré d'arrangement mixte Li/Ni.
(2) Le revêtement CP soulage le rétrécissement du paramètre de réseau c et supprime la transition de phase irréversible de H2-H3.
(3) La couche de revêtement CP inhibe les microfissures et la pulvérisation mécanique de la surface du matériau.
Cette étude montre que la couche de revêtement CP a un grand potentiel d'application dans la modification de surface des matériaux de cathode à ultra-haute teneur en nickel pour améliorer la stabilité du stockage du lithium, et fournit une nouvelle idée pour la stratégie d'optimisation de la stabilité électrochimique des matériaux de cathode à ultra-haute teneur en nickel. .
Matériel complémentaire
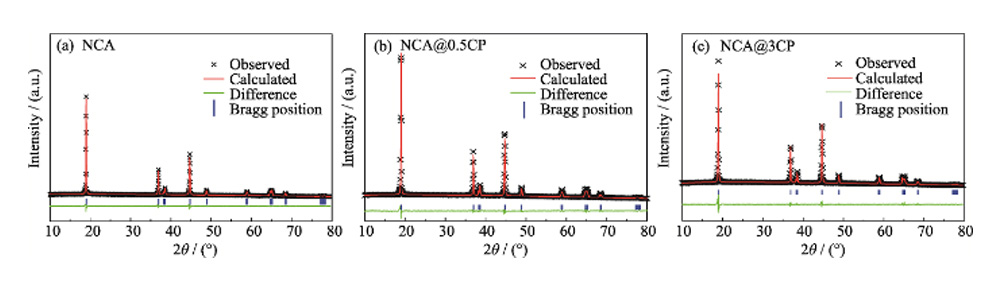

Fig. Images SEM S2 de (a, b) NCA, (c, d) NCA@0.5CP et (e, f) NCA@3CP
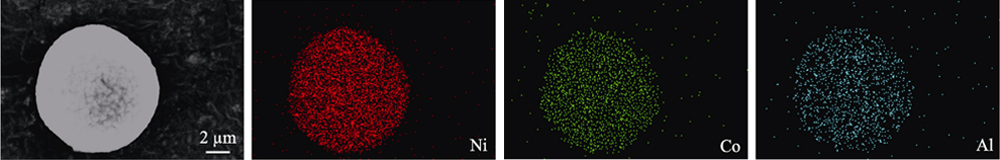
Fig. Cartographies élémentaires S3 EDS de NCA
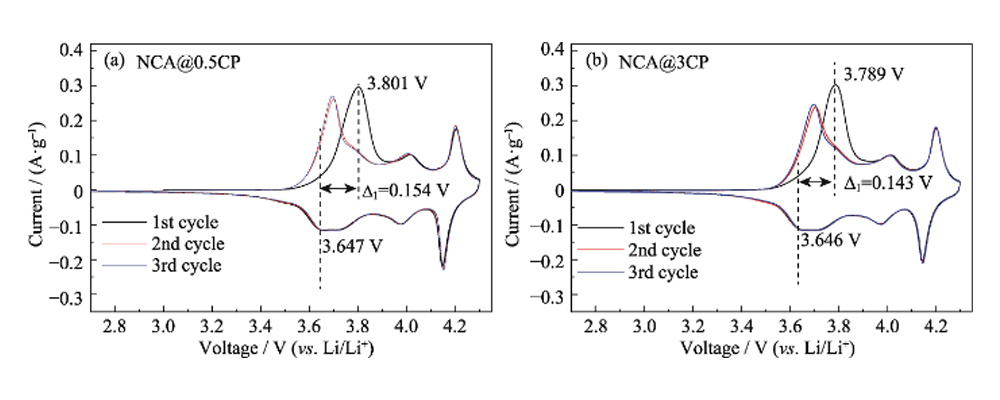
Fig. S4 Courbes CV pour (a) NCA@0.5CP et (b)NCA@3CP
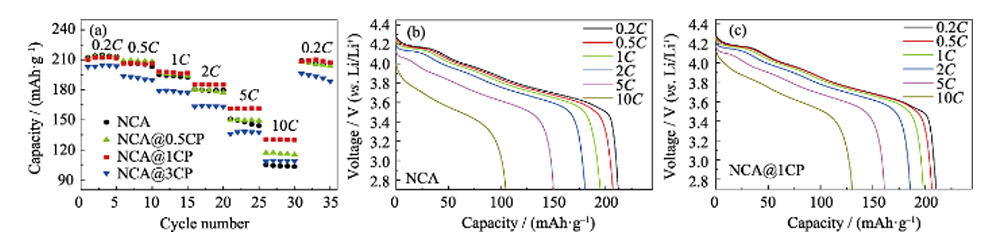
Fig. S5 (a) Performances tarifaires pour NCA, NCA@0.5CP, NCA@1CP et NCA@3CP ; Courbes de décharge correspondantes lors des tests de débit de (b) NCA et (c) NCA@1CP
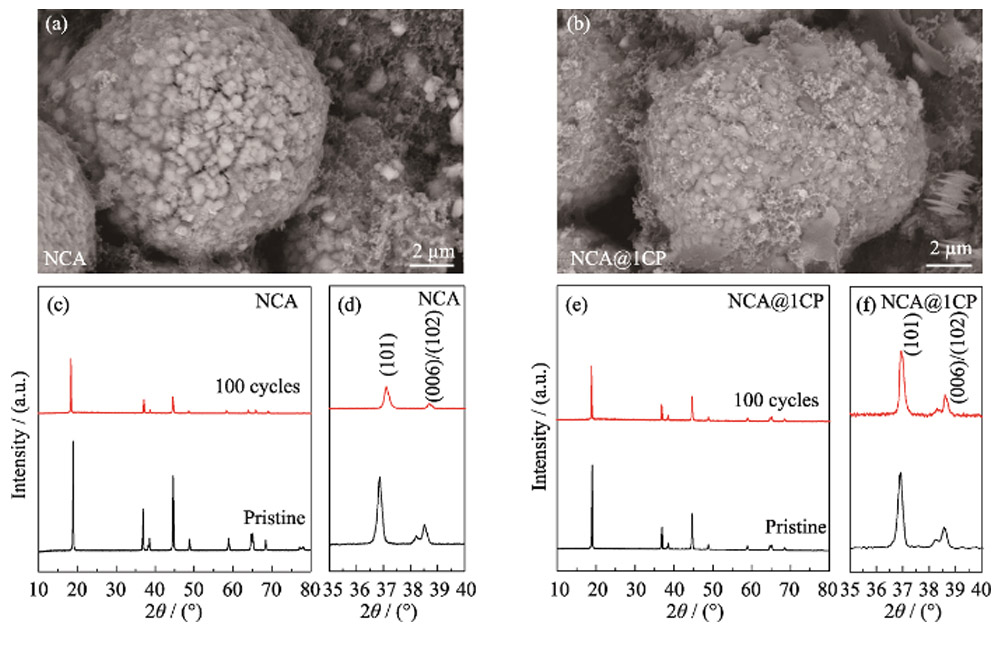
Fig. S6 (a, b) Images SEM et (cf) diagrammes XRD de NCA et NCA@1CP après 100 cycles sous 2,7-4,3 V à 1C
|
Goûter
|
ANC
|
NCA@0.5CP
|
NCA@1CP
|
N
CA@3CP
|
|
Je(003)/Je(104)
|
1.426
|
2.120
|
2.261
|
1.981
|
Tableau S2 Paramètres de réseau des NCA, NCA@0.5CP, NCA@1CP et NCA@3CP calculés à partir du raffinement XRD Rietveld
| Goûter | un/nm | c/nm | V/nm3 | Californie | Rwp | Rp |
| ANC | 0,287398 | 1.421071 | 0,101652 | 4.944609 | 7.13 | 4.18 |
| NCA@0.5CP | 0,287296 | 1.420733 | 0,101556 | 4.9451 88 | 6.63 | 4.73 |
| NCA@1CP | 0,287286 | 1.42044 | 0,101527 | 4.944341 | 5,86 | 4.39 |
| NCA@3CP | 0,287305 | 1.420646 | 0,101556 | 4.944731 | 6,74 | 4.82 |



