Matériau de cathode Na0.9Ni0.5Mn0.3Ti0.2O2 dopé au Sb de type O3 pour batterie Na-ion
KONG Guoqiang, LENG Mingzhe, ZHOU Zhanrong, XIA Chi, SHEN Xiaofang. Cathode Na0.9Ni0.5Mn0.3Ti0.2O2 de type O3 dopé au Sb Matériau pour batterie Na-ion [J]. Journal des matériaux inorganiques, 2023, 38(6) : 656-662.
Résumé
Mots clésï¼ Sb dopage; Type O3 ; matériau cathodique; méthode en phase solide ; tension large; Na-ion fabrication de batteries
Depuis la commercialisation du lithium-ion piles, elles ont été largement utilisées dans les appareils électroniques portables, électriques véhicules et stockage d’énergie électrochimique, etc. Cependant, le nombre limité Les ressources naturelles et la répartition inégale du lithium constituent un facteur limitant important le développement des batteries lithium-ion. Dans le même temps, les réserves de sodium sont abondante et largement distribuée, et plus important encore, en raison de la similitude des les propriétés chimiques du lithium et du sodium, le principe de fonctionnement de Les batteries sodium-ion sont proches de celles des batteries lithium-ion. Par conséquent, le application des batteries sodium-ion dans le domaine du stockage d'énergie à grande échelle a reçu une grande attention.
Matériaux cathodiques pour batteries sodium-ion
comprennent principalement des oxydes en couches de métaux de transition, des composés polyanioniques et
Analogues du bleu de Prusse. Parmi eux, l'oxyde en couches NaxTMO2 (TM fait référence à
métal de transition, 0
Parmi les différents matériaux NaxTMO2 de type O3 qui ont été rapportés, NaxTMO2 contenant Ni et Mn a attiré beaucoup attention en raison de ses abondantes ressources Ni/Mn et de sa grande capacité de stockage. Par exemple, le NaNi0,5Mn0,5O2 de type O3 a une capacité réversible élevée (133mAh gâ1). Bonnes performances (30C, 40mAh gâ1) et longue durée de vie (rétention de capacité spécifique de 70% après 500 cycles à 3,75C). Toutefois, certains problèmes subsistent qui limitent encore davantage son application. Développement, tel qu'une performance de débit insatisfaisante, une transition de phase complexe pendant la charge et la décharge, et la décroissance rapide de la capacité, en particulier à haute température tensions de 4,1 à 4,5 V. Des études récentes ont montré que le dopage partiel d'autres Les éléments peuvent améliorer efficacement la réversibilité de la transition de phase. Pour Par exemple, Na0.9Ni0.4Mn0.4Ti0.2O2 dopé au Ti a une phase O3-P3 plus réversible transition entre 2,5 et 4,2 V, capacité spécifique plus élevée (197 mAh g-1), et performances de cycle plus stables. NaFe0.2Mn0.4Ni0.4O2 dopé au Fe a un capacité réversible (165 mAh g-1) et une transition de phase stable (capacité 87% rétention après 200 cycles) dans la plage de 4,0 à 4,3 V.
De plus, le dopage Sb5+ peut également améliorer la stabilité du cycle et la tension de fonctionnement des matériaux cathodiques. Pour obtenir une structure matérielle plus stable et des performances supérieures dans un plage de tension plus large pour les oxydes en couches de type O3. Dans cette étude, Sb5+ était partiellement substitué au Ni2+ dans Na0.9Ni0.5Mn0.3Ti0.2O2 (NMT) par un simple méthode à l'état solide pour étudier l'effet du dopage au Sb sur les propriétés électrochimiques performances des oxydes en couches et changement de réversibilité de la phase O3-P3 transition dans une large plage de tension.
1 Méthode expérimentale
1.1 Préparation du matériau
Na0,9Ni0,5-xMn0,3Ti0,2SbxO2 (NMTSbx, x=0, 0,02, 0,04, 0,06) ont été préparés par la méthode en phase solide. Le spécifique Les étapes sont les suivantes : mélanger Na2CO3, NiO, Sb2O5, MnO2 et TiO2 dans le rapport stœchiométrique correspondant, et ajouter une fraction molaire supplémentaire de 5 % de Na2CO3 en tenant compte de la volatilité du Na à haute température. Broyez-le uniformément avec un mortier d'agate et à l'aide d'une machine à comprimés, réalisez un disque fin de Ï16 mm. Traitement thermique à 950 °C sous atmosphère d'air deux fois, à chaque fois pendant 12h. La même procédure a été utilisée pour préparer NMTSb0 sans démarrer Sb2O5. matériel, et tous les échantillons ont été stockés dans une boîte à gants pour une utilisation ultérieure.
1.2 Ensemble batterie
La matière active NMTSbx, le noir d'acétylène et le fluorure de polyvinylidène (PVDF) ont été pesés selon un rapport massique de 7:2:1, et une quantité appropriée de N-méthylpyrrolidone (NMP) a été ajoutée au broyage pour obtenir une bouillie uniformément mélangée. La boue a été enduite sur la surface d'aluminium feuille, et la charge superficielle du matériau actif dans l'électrode était d'environ 2,5 mg cm-2. Séché sous vide à 80°C pendant 12 h, puis découpé en petits disques de Ï12 mm avec un microtome comme électrode positive. Bouton CR2032 Les cellules ont été assemblées dans une boîte à gants remplie de gaz Ar (les fractions volumiques de l'eau et l'oxygène étaient tous deux inférieurs à 1 × 10-6). Parmi eux, la contre-électrode est une feuille de sodium métallique, le séparateur est en fibre de verre et l'électrolyte est de 1 mol L-1 NaClO4 solution de carbonate de dibutyle + carbonate de fluoroéthylène (volume rapport 1 : 1).
1.3 Caractérisation et tests des matériaux
Le spectre de diffraction des rayons X (XRD) du L'échantillon a été testé à l'aide du MiniFlex 600 (Rigaku, Japon, Cu Kα) et du cristal la structure a été affinée par Rietveld grâce à l'analyse structurelle système (GSAS + EXPGUI). La morphologie microscopique et la taille des particules du les échantillons ont été observés au microscope électronique à balayage JSM-7610F (JEOL, Japon) (SEM) et microscope électronique à transmission haute résolution JEOL JEM-2100F (HRTEM). La spectroscopie photoélectronique à rayons X (XPS) de l'état de valence du Les éléments ont été testés sur un spectromètre Escalab250xi en utilisant des rayons X achromatiques AlKα source. Le rapport molaire de chaque élément de l'échantillon a été analysé par spectromètre d'émission optique à plasma à couplage inductif (ICP-AES, iCAP 6300). Les mesures de charge et de décharge ont été effectuées à température ambiante à l'aide d'un Système de test de batterie Land CT2001A entre 2,0 et 4,2 V, et système électrochimique la spectroscopie d'impédance (EIS) des électrodes a été mesurée à l'aide d'un CHI660E poste de travail électrochimique (CH Instruments).
2 Résultats et discussion
2.1 Caractéristiques structurelles de NMTSbx
La composition élémentaire de tous les échantillons a été déterminé par ICP-AES et les résultats sont présentés dans le tableau S1. Au sein du plage d'erreur de mesure, le contenu réel de chaque ion métallique est essentiellement cohérent avec la composition de conception. Dans le spectre XRD de la figure 1 (a), tous les échantillons ont une structure hexagonale α-NaFeO2 de type O3 (groupe spatial R-3m), conforme à NaNi0,5Mn0,5O2 (JCPDS 54-0887). Il est montré que le l'introduction de Sb dans le réseau NMT ne modifie pas la structure intrinsèque du matériel. Le processus de préparation de cathodes d'oxyde en couches à haute teneur en nickel par la méthode à l'état solide produira inévitablement une petite quantité de résidus composants NiO inactifs, et la littérature montre que l'impact des traces les quantités de NiO sur les performances de la batterie sont négligeables. Sur la figure 1 (b), le les pics de diffraction de NMTSb0,02, NMTSb0,04 et NMTSb0,06 se sont déplacés vers de grandes angles et divers pics ont commencé à apparaître dans NMTSb0.06. Selon le Équation de Bragg (nλ=2dsinθ), la granulométrie moyenne de la poudre est qualitativement analysé. où n est l'ordre de diffraction, d est l'épaisseur moyenne (nm) des grains de l'échantillon perpendiculairement à la direction du cristal plan, θ est l'angle de diffraction correspondant à la plus forte diffraction pic, et λ est la longueur d’onde des rayons X (nm). Les résultats du calcul du plan cristallin montrent que la taille des grains de l’échantillon diminue après dopage au Sb, ce qui est lié à la différence de rayon ionique de Sb (0,06 nm) et Ni (0,069 n.m.). D’après le théorème de Vegard, cela signifie aussi qu’une solution solide la réaction s'est produite lors de la formation de NMTSbx.
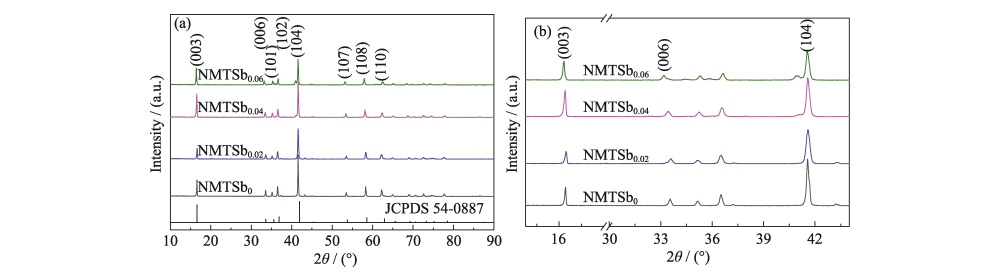
Fig. 1 Enquête (a) et (b) modèles XRD agrandis de NMTSbx (x = 0, 0,02, 0,04, 0,06)
La figure 2 (a, b) montre le XRD raffiné Modèles de Rietveld de NMTSb0 et NMTSb0.04 et paramètres de réseau détaillés sont présentés dans le tableau S2. On peut voir que les paramètres de réseau de NMTSb0.04 (a = b = 0,29790 nm) sont légèrement réduits par rapport au NMTSb0 d'origine (a = b = 0,29812 nm). Ceci est également attribué au fait que le rayon ionique de Sb (0,06 nm) est plus petit que celui du Ni (0,069 nm), ce qui est cohérent avec le Analyse DRX. Le c (c = 1,608391 nm) de NMTSb0,04 a été augmenté par rapport à celui de NMTSb0 (c = 1,600487 nm). La raison principale est que le paramètre de réseau a/b est sensible au changement de la longueur de la liaison (Ni/Mn/Ti/Sb)-O du plan basal de la structure en couches, et l'incorporation de Sb raccourcit la liaison longueur. Cela provoque la répulsion électrostatique entre les atomes d'oxygène dans le couche continue de métal de transition (Ni/Mn/Ti/Sb) pour devenir plus grande, conduisant à une augmentation de c. De plus, après calcul, le c/a de NMTSb0 et NMTSb0.04 a fait pas beaucoup changé, ils étaient respectivement de 5,36 et 5,39, tous deux supérieurs à 4,99, indiquant que les échantillons dopés ont conservé une bonne structure en couches.
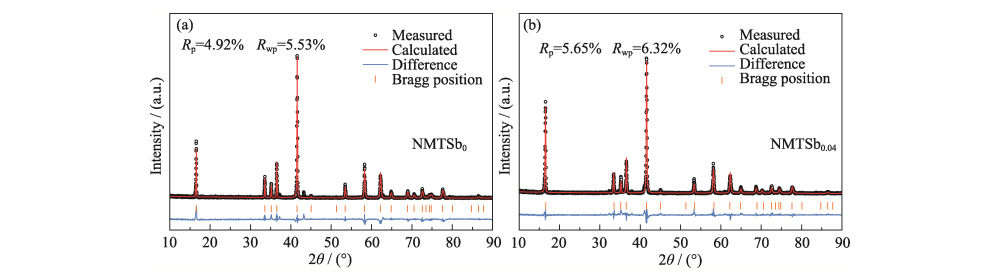
Fig. 2 Rietveld modèles XRD de raffinement de NMTSb0 (a) et NMTSb0.04(b)
La figure 3 montre les images SEM de NMTSb0 et NMTBSb0,04. Les deux produits sont composés d'un grand nombre de micro-nano-échelles disques minces avec une épaisseur uniforme et des bords clairs. Surtout après le dopage au Sb, la surface des flocons est plus lisse et les flocons hexagonaux ne manquent pas structure avec des bords et des coins vifs. Analyse élémentaire EDS sur zone sélectionnée de NMTSb0.04 montre que les éléments Na, O, Ni, Ti, Mn et Sb sont uniformément répartis dans l'échantillon, ce qui prouve également que les éléments Sb ont été dopés avec succès dans la structure intrinsèque de NMTSb0.

Fig. 3 SEM images et mappages EDS de NMTSb0 (a, b) et NMTSb0.04 (c, d)
Les microstructures de NMTSb0 et NMTSb0.04 ont été observés en outre par HRTEM et les résultats sont présentés à la figure S1. Dans Figure S1 (a, c), les particules avant et après dopage au Sb sont connectées ou superposées et apparaissent macroscopiquement comme une feuille ou approximativement structure circulaire ou polygonale. Les images HRTEM de la figure S1 (b, d) montrent le franges de réseau du matériau et les espacements de réseau de NMTSb0 et NMTSb0,04 sont respectivement de 0,238 et 0,237 nm. Les deux correspondent au (101) plan cristallin, et l'effet du dopage de Sb sur l'espacement du réseau est cohérent avec les résultats de l’analyse XRD. Les encadrés de la figure S1 (b, d) sont les points de le diagramme de diffraction électronique de zone sélectionnée (SEAD) de NMTSb0 et NMTSb0.04, ce qui prouve que les NMTSb0 et NMTSb0.04 obtenus ont une bonne cristallinité.
La spectroscopie photoélectronique à rayons X (XPS) de la figure S2 montre les résultats de l'état d'oxydation des éléments Mn, Ni, Ti et Sb dans NMTSb0 et NMTSb0.04. Sur la figure S2 (a), les deux principaux pics de NMTSb0 à 877 et 850 eV correspondent respectivement à Ni2p1/2 et Ni2p3/2, et tous deux appartiennent à Ni2+ dans l'échantillon. Le pic d'énergie de liaison à 858,2 eV est un satellite commun pic en élément Ni. Le Ni2p1/2 de NMTSb0.04 se divise en deux pics, indiquant que l'introduction de Sb dans le réseau NMTSb0 peut réduire le nombre de électrons externes autour de Ni, entraînant une forte délocalisation des électrons effet. Les métaux de transition ont des orbitales d plus délocalisées, ce qui peut améliorer l'interaction métal-métal des octaèdres à partage latéral MO6 dans les couches structure, inhibant ainsi l'effondrement des octaèdres MO6 et atténuant les réactions secondaires de l’oxygène et de l’électrolyte du réseau. Pendant le Processus de charge-décharge, la structure du matériau d'oxyde en couches devient plus stable, ce qui indique qu'une forte délocalisation électronique est bénéfique pour la stabilité structurelle de NMTSb0.04. Pour l'élément Mn, le Mn2p3/2 culmine à 642 eV et le pic Mn2p1/2 à 652 eV sur la figure S2 (b) indiquent la présence de Mn dans l'état de valence +4 dans NMTSb0 et NMTSb0.04. Le pic de Mn2p3/2 à 643eV peut être associé au pic Mn3+. La configuration octaédrique de Mn3+ sera déformé, ce qui est causé par la distorsion gingembre-Taylor. La dissolution de l'élément Mn entraînera une diminution rapide de la capacité, tandis que Ti dans NMTSb0,04 remplace une partie du Mn, et la réduction de la teneur en Mn peut également stabiliser le cadre structurel du matériau, inhibant ainsi le déclin rapide de capacité de la batterie causée par l’effet gingembre-Taylor. L'énergie de liaison typique pics de Ti2p1/2 et Ti2p3/2 à 457,3 et 453,1 eV pour NMTSb0 sur la figure S2(c) correspondent à l’état de valence +4 stable de Ti. Alors que les Ti2p1/2 et Ti2p3/2 les pics à 454,1 et 463,9 eV de NMTSb0,04 correspondent à Ti dans la valence +3 État. Du point de vue de la compensation des charges, cela est principalement dû à la réaction de réduction de Ti après l’introduction de Sb5+ à haute valence. Pendant la réaction de charge-décharge, Ti4+ a continué à exister sous une forme stable, ce qui a été vérifié dans la courbe de voltamétrie cyclique (CV) de NMTSb0,04, comme le montre Figure 4. Cela montre également que la source de capacité de la batterie n'a rien à voir avec le couple redox Ti4+/Ti3+. De plus, les pics d’énergie de liaison de NMTSb0,04 à 529 – 536 eV sur la figure S2 (d) confirme la présence de Sb.
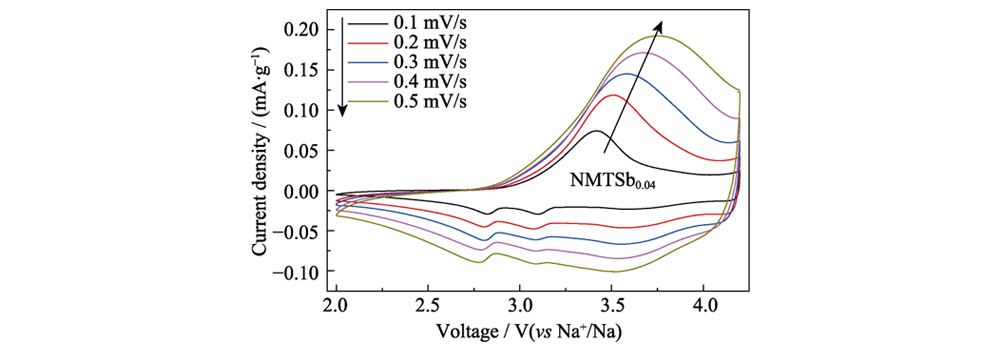
Fig. 4 CV courbes du matériau cathodique NMTSb0.04
2.2 Performances électrochimiques
La figure 5 montre le comportement électrochimique tracé de Nyquist d'impédance de NMTSbx. Parmi eux, le demi-cercle au milieu et La région haute fréquence représente la résistance de transfert de charge (Rct) entre L'électrolyte et l'électrode, et la ligne oblique dans la basse fréquence La région représente la résistance de Warburg provoquée par la diffusion du sodium ions. L'ajustement du circuit équivalent montre que le Rct de NMTSb0 et NMTSb0.04 sont 1185,4 et 761 Ω, respectivement. À mesure que le contenu dopant en Sb augmente, le l'impédance de l'échantillon diminue également. Lorsque x=0,04, l'impédance du L'échantillon atteint la valeur minimale. Augmenter encore la teneur en dopage Sb conduit à une augmentation de l’impédance. Lorsque x=0,06, l'impédance dépasse celle de l’échantillon NMTSb0. Un contenu de dopage approprié peut obtenir le métal optimal espacement intercouche de la structure en couches, assure un transport fluide des électrons Canaux, aident à améliorer les caractéristiques dynamiques de NMTSb0.04, et au en même temps, prendre en compte la stabilité de la structure globale.
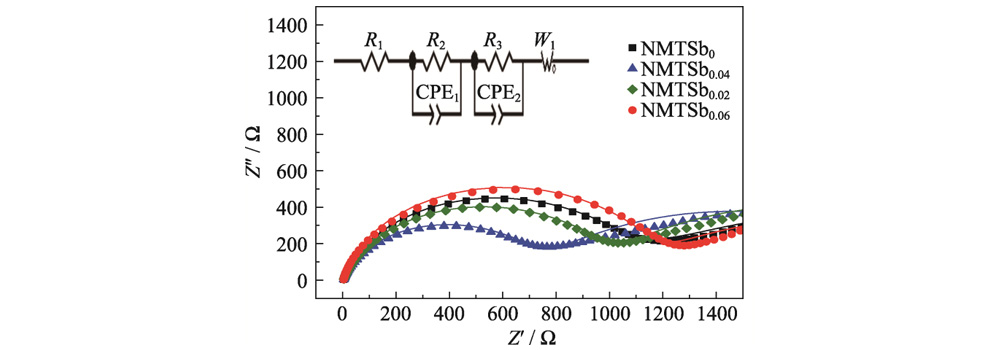
Fig. 5 Électrochimique spectres d'impédance de NMTSbx
Sous la condition de densité de courant de 1C (240 mA·gâ1) et plage de tension de 2,0 à 4,2 V, le sodium performances de stockage de la batterie Na-ion avec NMTSbx car l'électrode était testé. Comme le montre la figure 6(a), les capacités réversibles de NMTSbx (x=0, 0,02, 0,04, 0,06) sont respectivement de 122,8, 128,0, 135,2 et 103,9 mAh gâ1. La différence de capacité spécifique est due à contenu dopant différent. La stratégie de substitution d’éléments chimiques peut supprimer la transition de phase irréversible et améliorer le transport des ions sodium cinétique. Les avantages sont résumés comme suit : remplacez les produits hautement actifs éléments avec des éléments électrochimiquement inactifs et structurellement stables, tels que en empêchant le mélange de cations en augmentant la barrière énergétique de la migration du Ni2+, et réduire l'oxygène libéré pendant le cycle électrochimique en renforcer les liaisons métal-oxygène. Dopage ou remplacement des sites de métaux de transition peut inhiber de manière significative la transition de phase, inhiber l'ion du métal de transition Migration et améliorer la stabilité chimique et électrochimique de matériaux désodiques. Le contenu spécifique du dopage devrait être exploré selon le type d'élément dopant et la structure intrinsèque. . Sur le d'une part, le dopage avec des ions métalliques de haute valence peut améliorer la conductivité globale du matériau après que les ions métalliques pénètrent à l’intérieur du réseau. Quand la fraction molaire de dopage est supérieure à 1% (rapport stoechiométrique x0,01), la résistivité diminuera rapidement, ce qui aura un grand influence sur la conductivité. D’un autre côté, une quantité de dopage trop élevée entraînera réduira inévitablement le contenu des couples redox dans le système et affectera le densité énergétique du système, alors qu'une quantité trop faible de dopage ne suffira pas pour stabiliser la structure des matériaux d'oxyde en couches. Dans cette étude, NMTSbx(x=0, 0,02, 0,04, 0,06), x est le rapport stœchiométrique et le réel la teneur en dopage est respectivement de 2 %, 4 % et 6 % en fraction molaire.
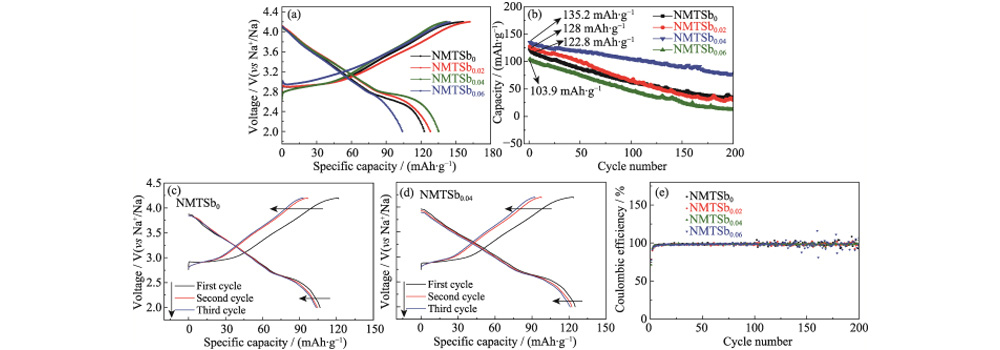
Fig. 6 Performances de batteries Na-ion avec NMTSbx comme électrodes
(a) Chargement et courbes de décharge de batteries Na-ion avec des échantillons comme électrodes pour la première cycle à 1C ; (b) Performances de cyclage des batteries Na-ion avec des échantillons comme électrodes à 1 C pendant 200 cycles ; (c, d) Chargement et déchargement courbes de batteries Na-ion avec des échantillons comme électrodes pour les 3 premiers cycles à 5C ; (e) Efficacité coulombienne des batteries Na-ion avec NMTSbx comme électrodes pour 200 cycles à 1C Des figures colorées sont disponibles sur site Internet
Sur la figure 6 (a), la courbe charge-décharge de l'échantillon non dopé NMTSb0 contient évidemment plusieurs plateaux de tension et étapes, indiquant que plusieurs transitions de phase de l'hexagone à la monoclinique peut apparaître dans la structure en couches. Cependant, alors que le glissement de la couche intermédiaire du Une couche de métal de transition se produit, la courbe globale de charge-décharge est relativement lisse. Les trois plateformes de tension au-dessus de 3,00 V ont tendance à être floues. Pour NMTSb0, la courbe de charge est principalement divisée en deux parties : la section de pente autour de 3,00-3,80 V et la section longue plateau au-dessus de 3,80 V. Cependant, lorsque Sb a été introduit, la tension initiale du segment de plate-forme a augmenté au-dessus 4,00 V. Pour la courbe de décharge, le long plateau se produit généralement dans la tension plage de 2,50 à 2,75 V. L'apparition du plateau de tension peut être attribuée à la transformation de la phase O3 en phase P3, tandis que la pente Le segment lorsque la tension augmente est provoqué par la réaction de la solution solide avec la structure P3. La figure 6 (b) est une comparaison des performances du cycle de Électrodes NMTSbx (x = 0, 0,02, 0,04, 0,06) à une densité de courant de 1C. C'est Il convient de noter que la stabilité cyclique du matériau cathodique NMTSb0.04 est la meilleur, et environ 70 % de la capacité réversible peut être conservée après 200 cycles. En revanche, la capacité spécifique de l’électrode NMTSb0 diminue considérablement. rapidement, avec une valeur initiale de 122,8 mAh g-1, qui descend à 51 mAh g-1 après 200 cycles, il ne reste que 41,5 % de la capacité spécifique. Sur la figure 6(c, d), même à un taux très élevé de 5C (1200 mA gâ1), le la rétention de capacité spécifique de l'électrode NMTSb0.04 est toujours de 92,6 % (125,3 mAh gâ1). La capacité spécifique du NMTSb0 l'électrode n'est que de 106,7 mAh·gâ1, ce qui est supérieur à d'autres oxydes en couches de type O3 signalés. La capacité spécifique de décharge initiale de O3-Na(Ni1/3Mn1/3Fe1/3)0,95Al0,05O2 préparé par le groupe de Yan à raison de 0,1C est de 145,4 mAh·gâ1. Et après 80 cycles à 0,2C, le spécifique réversible la capacité est de 128,4 mAh·gâ1. Le O3-NaNi0,5Mn0,5O2 préparé par le groupe de recherche de Guo a une capacité spécifique de 80 mAh·g-1 dans la plage de tension de 2-4 V à un taux de 2C. La figure 6 (e) présente l'efficacité coulombienne du Batterie Na-ion pendant un cycle continu à 1C. Parmi eux, les Coulombiens La distribution d'efficacité de l'électrode NMTSb0.04 est stable et tend vers une ligne droite, se maintenant essentiellement à 98 %, ce qui indique également que son la structure en couches est plus stable. Cependant, l'efficacité coulombienne du L'électrode NMTSb0 a fluctué considérablement après 140 cycles, et il y avait un grand saut alors qu'il était proche de 200 cycles. La batterie assemblée avec NMTSb0,04 après 200 cycles a été démonté et traité, et le spectre XRD de la feuille d'électrode a été testée, les résultats sont présentés à la figure S3. Le DRX les pics de diffraction de la pièce polaire NMTSb0,04 ne se sont pas déplacés de manière significative après cyclage, indiquant que le changement de phase irréversible de la cathode NMTSb0.04 le matériel a été supprimé après le dopage.
3 Conclusion
Dans cette étude, Na0.9Ni0.5-xMn0.3Ti0.2SbxO2 (NMTSbx, x = 0, 0,02, 0,04, 0,06), un matériau de cathode d'oxyde en couches pour batteries sodium-ion, a été préparée par une méthode pratique à l’état solide. C'est les particules sont composées de flocons à l'échelle micro-nano avec une épaisseur uniforme et des bords clairs et la taille des grains diminue après que Sb remplace une partie de Ni. Au Dans le même temps, le dopage du Sb provoque une forte délocalisation des électrons, ce qui réduit l'énergie de l'ensemble du système et obtient une structure stable qui est plus propice aux cycles de charge-décharge à long terme. Dans le domaine électrochimique test dans la plage de 2,00 à 4,20 V, le dopage au Sb a supprimé la phase irréversible transition du matériau de la cathode et amélioration de la plate-forme de tension de fonctionnement. Lorsqu'il est chargé et déchargé au taux 1C, la capacité spécifique de décharge initiale de NMTSb0,04 est de 135,2 mAh·g-1, et le taux de rétention de capacité après 200 cycles est de 70 %. La rétention de capacité spécifique peut atteindre 92,6 % (125,3 mAh·gâ1) à un taux de 5C.
Informations supplémentaires

Fig. S1 HRTEM images de NMT (a, b) et NMTSb0.04 (c, d) avec encart en (b, d) montrant les images SEAD correspondantes
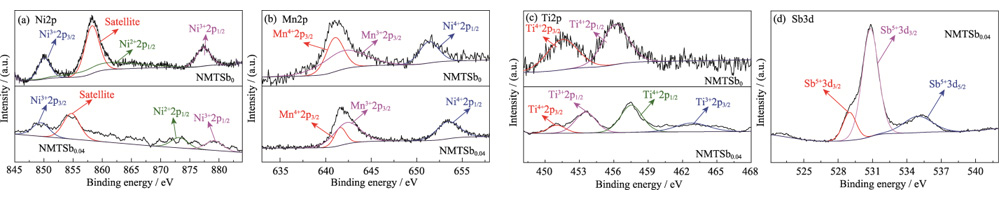
Fig. S2 (a) Spectres XPS Ni2p, (b) Mn2p, (c) Ti2p et (d) Sb3d de NMTSb0 et NMTSb0.04
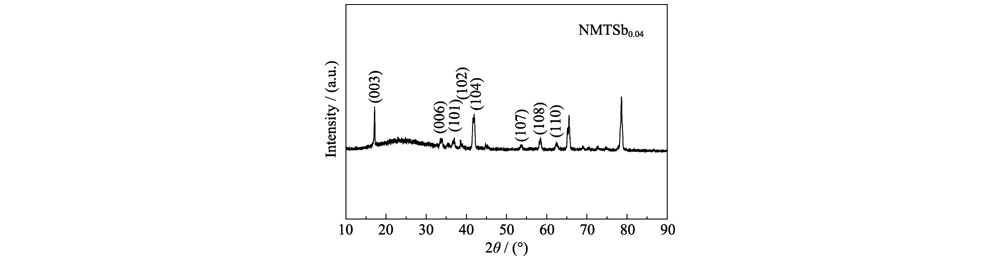
Fig. S3 DRX modèle de NMTSb0.04 comme matériau de cathode de Batterie Na-ion après 200 cycles
Tableau S1 Résultats ICP-AES de O3-NMTSbx (x = 0, 0,02, 0,04, 0,06) (rapport stœchiométrique)
|
Na |
Ni |
Mn |
Ti |
Sb |
|
|
NMTSb0 |
0,913 |
0,486 |
0,288 |
0,181 |
0 |
|
NMTSb0.02 |
0,924 |
0,471 |
0,284 |
0,186 |
0,023 |
|
NMTSb0.04 |
0,920 |
0,452 |
0,287 |
0,184 |
0,039 |
|
NMTSb0.06 |
0,929 |
0,435 |
0,279 |
0,184 |
0,061 |
Tableau S2 Paramètres de réseau des matériaux avec NMTSb0 et NMTSb0.04
|
a/nm |
b/nm |
c/nm |
V/nm3 |
RP/% |
Rp/% |
|
|
NMTSb0 |
0,29812 |
0,29812 |
1.600487 |
0,1232 |
4,92 |
5,53 |
|
NMTSb0.04 |
0,29790 |
0,29790 |
1.608391 |
0,1236 |
5,65 |
6,32 |