Catégories
nouveau blog
- Guide de sélection des électrolytes pour batteries : ce que les responsables des achats doivent savoir
- Équipement de laboratoire pour piles bouton : la liste de contrôle complète pour les laboratoires de R&D sur les batteries
- Comparaison des matériaux de cathode pour batteries : NMC, LFP et NCA
- Tendances de fabrication des batteries lithium-ion 2026 : Guide d’achat B2B
- Guide étape par étape du processus de fabrication des batteries lithium-ion
Tags
Électrolytes céramiques Na3Zr2Si2PO12 pour batterie Na-ion
Na3Zr2Si2PO12 Céramique Électrolytes pour batterie Na-ion : préparation par méthode de séchage par pulvérisation et ses Propriété
Auteurs : LI Wenkai, ZHAO Ning, BI Zhijie, GUO Xiangxin. Électrolytes céramiques Na3Zr2Si2PO12 pour batterie Na-ion : préparation à l'aide Méthode de séchage par pulvérisation et ses propriétés. Journal des matériaux inorganiques, 2022, 37(2) : 189-196 DOI :10.15541/jim20210486
Résumé
Les batteries Na-ion, qui utilisent actuellement des matières organiques inflammables et explosives électrolytes, il est désormais urgent de développer des solides à ions sodium de haute performance Électrolyte pour réaliser une application plus sûre et plus pratique. Na3Zr2Si2PO12 est l'un des électrolytes de sodium solides les plus prometteurs pour sa large fenêtre électrochimique, résistance mécanique élevée, stabilité de l'air supérieure et conductivité ionique élevée. Mais son mélange inhomogène des particules céramiques avec les liants provoquant beaucoup plus de pores dans les corps verts rendent difficile l'obtention d'une haute densité et des électrolytes céramiques à haute conductivité après frittage. Ici, le spray La méthode de séchage a été utilisée pour permettre aux particules Na3Zr2Si2PO12 uniformément enduit de liants et granulé en secondaires sphériques. Le les particules distribuées normales telles que préparées peuvent entrer en contact efficacement les unes avec les autres et réduire la porosité du corps vert en céramique. Après frittage, céramique Na3Zr2Si2PO12 les pellets via le séchage par pulvérisation présentent une densité relative de 97,5 % et conductivité ionique de 6,96 × 10-4 Sâcm-1 dans la pièce température. En revanche, la densité relative et la température ambiante conductivité ionique des pastilles de céramique Na3Zr2Si2PO12 préparés sans séchage par pulvérisation ne sont que de 88,1 % et 4,94 × 10-4 Sâcm-1, respectivement.
Mots clésï¼ électrolyte solide ; méthode de séchage par pulvérisation ; densité; conductivité ionique; Na3Zr2Si2PO12
Les ions sodium et les ions lithium appartiennent tous deux à le premier groupe principal, ont des propriétés chimiques et une intercalation similaires mécanismes et sont riches en réserves de ressources. Par conséquent, les batteries sodium-ion peut compléter les batteries lithium-ion [1, 2, 3]. Batteries sodium-ion contenant les électrolytes organiques inflammables et volatils présentent des problèmes de sécurité et des risques limités densité énergétique. Si des électrolytes solides sont utilisés à la place des électrolytes liquides, les problèmes de sécurité devraient être résolus [4,5,6,7,8]. Électrolytes solides inorganiques avoir une large fenêtre électrochimique et peut être associé à une cathode haute tension matériaux, augmentant ainsi la densité énergétique des batteries [9]. Cependant, les électrolytes solides sont confrontés à des défis tels qu'une faible conductivité ionique et des difficultés transmission ionique à l’interface entre électrodes et électrolytes. Alors que pour optimiser l'interface, il faut d'abord trouver des électrolytes solides avec conductivité ionique élevée [10, 11, 12].
À l'heure actuelle, l'ion sodium le plus étudié les électrolytes solides inorganiques comprennent principalement Na-βâ-Al2O3, de type NASICON et sulfure. Parmi eux, les ions rapides de type NASICON (Sodium Super Ion Conductors). les conducteurs ont un grand potentiel dans les applications de batteries sodium-ion à semi-conducteurs grâce à leur large fenêtre électrochimique, leur haute résistance mécanique, leur stabilité à l'air et une conductivité ionique élevée [13,14] . Il a été initialement rapporté par Goodenough et Hong et al. [15,16]. La formule générale est Na1+xZr2SixP3-xO12 (0â¤xâ¤3), qui est une solution solide continue formée par NaZr2(PO4)3 et Na4Zr2(SiO4)3 et possède un canal de transmission Na+ tridimensionnel ouvert. Na1+xZr2SixP3-xO12 a deux structures : structure en losange (R-3c) et monoclinique structure (C2/c, 1,8â¤xâ¤2,2). Lorsque x = 2, Na3Zr2Si2PO12 a le niveau ionique le plus élevé conductivité. À 300 â, la conductivité ionique du Na3Zr2Si2PO12 peut atteindre 0,2 Sâcm-1, ce qui est proche de la conductivité ionique du Na-βâ-Al2O3 (0,1~ 0,3 Sâcm-1) [15]. L'ion à température ambiante actuelle la conductivité de Na3Zr2Si2PO12 rapportée dans la littérature [17,18] est environ ~10-4 Sâcm-1. Dopage des éléments les méthodes sont couramment utilisées pour améliorer la conductivité ionique. Depuis le solide NASICON L'électrolyte a une structure à squelette ouvert, il peut être dopé avec une variété de éléments. Par exemple, les éléments qui remplacent Zr4+ incluent Mg2+, Zn2+, Al3+, Sc3+, Y3+, La3+, Ti4+, Hf 4+, Nb5+, Ta5+, etc. [17, 18, 19, 20, 21, 22]. Ceux le remplacement de P5+ inclut Ge5+ et As5+ [22]. En plus du dopage élémentaire, augmenter la densité des feuilles de céramique Na3Zr2Si2PO12 est également une méthode courante pour améliorer leur conductivité ionique. Récemment, Yang et al. [18] élément utilisé dopage combiné à un frittage sous atmosphère d'oxygène pour synthétiser des dense Na3.2+2xZr2-x ZnxSi2.2P0.8O12 (0â¤xâ¤0,15). Lorsque x=0,1, la pièce la conductivité ionique de la température atteint la valeur maximale (5,27 × 10-3 Sâcm-1). Les méthodes de préparation de l'électrolyte céramique Na3Zr2Si2PO12 inclure : frittage conventionnel (CS), frittage en phase liquide (LPS), étincelle frittage plasma (SPS), frittage par micro-ondes (MWS) et processus de frittage à froid (CSP) [18-21,23-29]. Parmi eux, Huang et al. [20] a utilisé le frittage conventionnel méthodes pour augmenter la densité des céramiques par dopage Ga3+. Une céramique un électrolyte avec une conductivité ionique à température ambiante plus élevée (1,06 × 10-3 Sâcm-1) et une conductivité électronique plus faible (6,17 × 10-8 Sâcm-1) a été obtenu. ZHANG et coll. [21] a adopté le frittage conventionnel méthode en introduisant le cation La3+. La phase intermédiaire Na3La(PO4)2 se forme au joint de grain, et une feuille de céramique Na3.3Zr1.7La0.3Si2PO12 avec un une densité aussi élevée que 99,6 % est obtenue. L'ion correspondant à température ambiante la conductivité peut atteindre 3,4 × 10-3 Sâcm-1. WANG et coll. [23] utilisé frittage par micro-ondes (MWS) pour obtenir des céramiques Na3Zr2Si2PO12 à haute densité de 96 % à une basse température de frittage de 850 °C et maintenu seulement pendant 0,5 h, réduisant ainsi le frittage frais. Les valeurs de densité relative (rrelative), de conductivité ionique (Ït) et énergie d'activation (Ea) des électrolytes céramiques préparés par différentes méthodes sont répertoriés dans le tableau 1.
Tableau 1 Paramètres clés de type NASICON matériaux pour différentes méthodes de frittage
|
Méthode de frittage |
Composition |
Frittage |
Frittage |
Heure/h |
relatif/% |
st/(Sâcm-1) |
Ea/eV |
Réf. |
|
CSP |
Na3,256Mg0,128Zr1,872Si2PO12 |
140 |
Aucun |
1 |
82,9 |
0,41´10-4 |
- |
[19] |
|
FH-CSP |
Na3Zr2Si2PO12 |
375 |
NaOH |
3 |
93 |
2.2´10-4 |
0,32 |
[24] |
|
LPS |
Na3Zr2Si2PO12 |
1150 |
NaF |
24 |
- |
1.7´10-3 |
0,28 |
[25] |
|
LPS |
Na3Zr2Si2PO12 |
900 |
Na3BO3 |
10 |
93 |
1.4´10-3 |
- |
[26] |
|
LPS |
Na3Zr2Si2PO12 |
1175 |
Na3SiO3 |
10 |
93 |
1.45´10-3 |
- |
[27] |
|
SPS |
Na3.4Zr1.6Sc0.4Si2PO12 |
1100 |
KOHaq |
0,1 |
95 |
9.3´10-4 |
- |
[28] |
|
SPS |
Na3Zr2Si2PO12 |
1210 |
Aucun |
0,5 |
97,0 |
1.7´10-3 |
0,28 |
[29] |
|
MWS |
Na3Zr2Si2PO12 |
850 |
Aucun |
0,5 |
96 |
2,5´10-4 |
0,31 |
[23] |
|
CS |
Na3Zr2Si2PO12 |
1250 |
Aucun |
16 |
71,4 |
1.7´10-4 |
0,36 |
[20] |
|
CS |
Na3.1Zr1.9Ga0.1Si2PO12 |
1250 |
Aucun |
16 |
86,5 |
1.06´10-3 |
0,29 |
[20] |
|
CS |
Na3Zr2Si2PO12 |
1200 |
Aucun |
24 |
87,6 |
6.7´10-4 |
0,353 |
[21] |
|
CS |
Na3.3Zr1.7La0.3Si2PO12 |
1200 |
Aucun |
24 |
99,6 |
3.4´10-3 |
0,291 |
[21] |
|
CS |
Na3Zr2Si2PO12 |
1250 |
Aucun |
- |
84.02 |
2.17´10-4 |
0,407 |
[18] |
|
O2-CS |
Na3.4Zr1.9Zn0.1Si2.2P0.8O12 |
1250 |
Aucun |
- |
99,46 |
5.27´10-3 |
0,285 |
[18] |
|
CS |
Na3Zr2Si2PO12 |
1250 |
Aucun |
6 |
88,1 |
4.94´10-4 |
0,34 |
Cet ouvrage |
|
SD-CS |
Na3Zr2Si2PO12 |
1250 |
Aucun |
6 |
97,5 |
6,96´10-4 |
0,32 |
Cet ouvrage |
CS : frittage classique ; SD : séchage par pulvérisation ; O2-CS : frittage conventionnel en pur oxygène; CSP : procédé de frittage à froid ; FH-CSP : frittage à froid d'hydroxydes fondus processus; MWS : frittage par micro-ondes ; LPS : frittage en phase liquide ; SPS : étincelle frittage plasma
Les méthodes conventionnelles utilisent de la poudre préparée par frittage direct pour mélanger avec un liant pour produire de la poudre de corps céramique, puis subir un moulage de poudre et un frittage à haute température pour obtenir des céramiques [30, 31, 32]. Cependant, pendant le processus de broyage et de mélange, en raison d'un mélange inégal du liant et des particules de céramique et un mauvais contact entre les particules, il il y a de nombreux pores à l'intérieur du corps vert, ce qui rend difficile la préparation de la céramique électrolytes à haute densité et haute conductivité ionique. Le séchage par pulvérisation est un méthode de séchage rapide qui utilise un atomiseur pour disperser la bouillie en gouttelettes et utilise de l'air chaud pour sécher les gouttelettes afin d'obtenir de la poudre. Les particules du la poudre préparée par séchage par pulvérisation est sphérique et le liant peut être uniformément déposé à la surface des particules [33]. KOU et coll. [34] utilisé le séchage par pulvérisation combiné avec un frittage à haute température pour synthétiser un électrolyte solide Li1.3Al0.3Ti1.7SixP5(3-0.8x)O12 (LATSP) avec ionique à haute température ambiante conductivité. Lorsque x=0,05, la conductivité ionique à température ambiante atteint un maximum de 1,053 × 10-4 S × cm-1, et le compacté la densité est de 2,892 gâcm-3, ce qui est proche de la densité théorique de LATSP de 2,94 gâcm-3. On peut voir que le séchage par pulvérisation a certains avantages dans l'amélioration de la densité et de la conductivité ionique de la céramique électrolytes. Compte tenu des avantages du séchage par pulvérisation, l'effet de l'élément un dopage sur la densité céramique et la conductivité ionique doit être envisagé. Ce l'étude a sélectionné Na3Zr2Si2PO12 comme objet de recherche et a introduit le spray méthode de granulation dans la préparation préliminaire de matériaux en poudre pour préparer un électrolyte céramique Na3Zr2Si2PO12 à haute densité et à haute teneur ionique conductivité.
1 Méthode expérimentale
1.1 Préparation du matériel
Méthode de préparation de la poudre Na3Zr2Si2PO12 : Peser Na2CO3 (Aladdin, 99,99 %), NH4H2PO4 (Aladdin, 99 %), ZrO2 (Aladdin, 99,99%), et SiO2 (Aladdin, 99,99%) selon le rapport stœchiométrique. Dans afin de compenser la volatilisation de Na et P lors du frittage processus, la matière première contient un excès de 8% de Na2CO3 et 15% d'excès de NH4H2PO4 [25]. Des billes de zircone ont été utilisées comme milieu de broyage à billes, le Le rapport matériau/poids de la bille était de 1:3, de l'éthanol absolu a été utilisé comme dispersion milieu, et le broyeur à boulets a été utilisé pour le broyage à boulets pendant 12 h. Le broyeur à boulets La bouillie a été séchée dans une étuve à 80 °C pendant 12 h. La poudre séchée a été broyée et passé à travers un tamis de 150 mesh (100 μm), puis transféré dans un récipient à 400 °C creuset en alumine pendant 2 h. Retirer le CO32- et le NH4+ du précurseur, puis chauffer jusqu'à 1 000 ~ 1 150 °C pour la calcination et recuit-le après 12 heures pour obtenir Poudre Na3Zr2Si2PO12.
Méthode de préparation de la céramique Na3Zr2Si2PO12 feuilles : Afin d'explorer l'effet de la taille des particules de Na3Zr2Si2PO12 sur la densité des feuilles de céramique, deux séries d'expériences de contrôle ont été conçues. Le le premier groupe a utilisé des méthodes conventionnelles, en ajoutant 2 % (fraction massique) de polyvinyle liant alcool (Aladdin, Mw ~ 205000) à la poudre Na3Zr2Si2PO12 en phase pure, en ajoutant éthanol absolu et broyage à boulets pendant 12 h. La poudre après broyage à boulets est séché, broyé et tamisé pour obtenir une poudre recouverte d'un liant sur la particule surface. La poudre est pressée uniaxialement à froid à 200 MPa à l'aide d'un acier inoxydable. moule en acier pour fabriquer un corps vert de Ï12 mm, enregistré comme GB. . Afin de réduire la volatilisation de Na et P lors du processus de frittage des feuilles de céramique, le corps vert a été enterré dans la poudre mère et fritté à 1250°C pendant 6 heures puis recuit à une vitesse de chauffage de 4°C/min. L'obtenu L'électrolyte céramique Na3Zr2Si2PO12 a été désigné CS-NZSP. Le deuxième groupe utilisé un séchoir par pulvérisation (ADL311S, Yamato, Japon) pour granuler la poudre de Na3Zr2Si2PO12. Ajouter 2 % (fraction massique) de liant d'alcool polyvinylique (Aladdin, Mw ~ 205 000) et 2 % dispersant du polyéthylène glycol (Aladdin, Mn=1000) à la poudre Na3Zr2Si2PO12, et ajoutez de l'éthanol absolu. Préparer une suspension avec une teneur en solides de 15 % en masse fraction et broyeur à boulets pendant 12 h. La suspension broyée à boulets a été séchée par pulvérisation avec une température d'entrée de 130°C et un débit d'alimentation de 5 mL/min. Le La poudre de Na3Zr2Si2PO12 a été collectée à travers un séparateur à cyclone. Le comprimé et les procédés de frittage de céramique étaient les mêmes que ceux du premier groupe, et le corps vert Na3Zr2Si2PO12 obtenu et l'électrolyte céramique ont été enregistrés comme SD-GB et SD-CS-NZSP respectivement. Traitement de polissage de surface de la céramique carrelage : utilisez d'abord du papier abrasif de 400 mesh (38 μm) pour un polissage grossier, puis utilisez du papier abrasif de 1 200 mesh (2,1 μm) pour un polissage fin jusqu'à ce que la céramique la surface est lisse. Les diamètres de l'électrolyte céramique CS-NZSP et SD-CS-NZSP les feuilles mesurent respectivement (11,3 ± 0,1) et (10,3 ± 0,1) mm, et l'épaisseur est (1,0 ± 0,1) mm.
1.2 Caractérisation physique des matériaux
L'analyse de phase des échantillons a été réalisée à l'aide d'un diffractomètre à rayons X (XRD, Bruker, D8 Advance). Le la source de rayonnement est CuKα, la pression du tube est de 40 kV, le débit du tube est de 40 mA, la vitesse de balayage est de 2 (°)/min et la plage de balayage est de 2θ= 10°~80°. Balayage microscope électronique (MEB, Hitachi, S-4800) et microscope électronique à transmission (TEM, JEOL, JEM-2100F) ont été utilisés pour analyser la morphologie des échantillons, et l'accessoire EDX configuré a été utilisé pour l'analyse élémentaire.
1.3 Mesure de conductivité électrique de feuilles de céramique
La spectroscopie d'impédance électrochimique (EIS) de l’échantillon a été testé à l’aide d’un poste de travail électrochimique. L'épreuve la plage de fréquences est de 7 MHz ~ 0,1 Hz, la tension appliquée est de 10 mV, la courbe de test est installé et la conductivité ionique de la pièce en céramique est calculée à l'aide de formule (1).
Ï=L/(RÃS) (1)
Dans la formule, L est l'épaisseur du feuille de céramique (cm), R est la résistance (Ω), S est la zone de l'électrode de blocage (cm2), et Ï est la conductivité ionique (Sâcm-1).
La conductivité électronique de l'échantillon a été testé en utilisant une polarisation en courant continu (DC), avec une tension constante de 5 V et une durée de 5000 s. La valeur ordonnée après que la courbe soit devenue stable est la valeur du courant de polarisation. Utilisez les formules (2, 3) pour calculer le conductivité électronique et indice de migration des ions sodium de la feuille de céramique.
Ïe=LÃI/(VÃS) (2)
t=(Ï-Ïe)/Ï (3)
Dans la formule, L est l'épaisseur du feuille de céramique (cm), I est le courant de polarisation (A), V est la tension (V), S est la surface de l'électrode de blocage (cm2) et Ïe est la conductivité électronique (Sâcm-1). Ce travail utilise Au comme électrode de blocage. Préparation de Électrode de blocage : utiliser un équipement de revêtement par évaporation résistant au vide poussé (VZZ-300) pour évaporer la source d'évaporation Au grâce au chauffage par résistance, et évaporez-le sur la surface de la feuille de céramique. La feuille de céramique est fixé dans une virole d'un diamètre intérieur de 8 mm.
2 Résultats et discussion
2.1 Structure et morphologie des phases caractérisation de Na3Zr2Si2PO12
Afin d'optimiser le frittage température de Na3Zr2Si2PO12, la poudre a été frittée à 1000, 1050, 1100 et 1150 â respectivement. Les diagrammes de diffraction des rayons X des échantillons obtenus sous différentes températures de frittage sont illustrés à la figure 1. On peut voir d'après la figure que lorsque la température de frittage est de 1000°C, la phase principale de Na3Zr2Si2PO12 a été généré, mais il y a des impuretés Na2ZrSi2O7 et ZrO2 Phases, et l'intensité maximale de diffraction de la phase principale est faible et le la largeur du demi-pic est large, ce qui indique que le produit de frittage a une mauvaise qualité cristallinité. Lorsque la température de frittage est de 1100°, l'impureté ZrO2 La phase disparaît et l'intensité du pic de diffraction de l'impureté Na2ZrSi2O7 La phase s'affaiblit, indiquant qu'il est nécessaire d'augmenter la température de frittage. bénéfique pour éliminer la phase d’impuretés. Les pics de diffraction du les produits frittés à 1100 et 1150 °C ont des largeurs de demi-pic plus petites que les pics de diffraction des produits frittés à 1000°C, indiquant que le plus la température de frittage est élevée, meilleure est la cristallinité du produit. Par rapport au produit fritté 1000 â, les pics de diffraction du 1150 â les produits frittés sont divisés à 2θ = 19,2°, 27,5° et 30,5°. Cela montre que le le matériau passe d'une phase rhombique à faible conductivité ionique à une phase monoclinique à haute conductivité ionique [25,35]. Et le pic de diffraction est conforme au pic de diffraction standard PDF 84-1200, indiquant que 1 150 °C est la température de formation de phase de l'électrolyte solide Na3Zr2Si2PO12. avec une structure monoclinique à haute conductivité ionique.
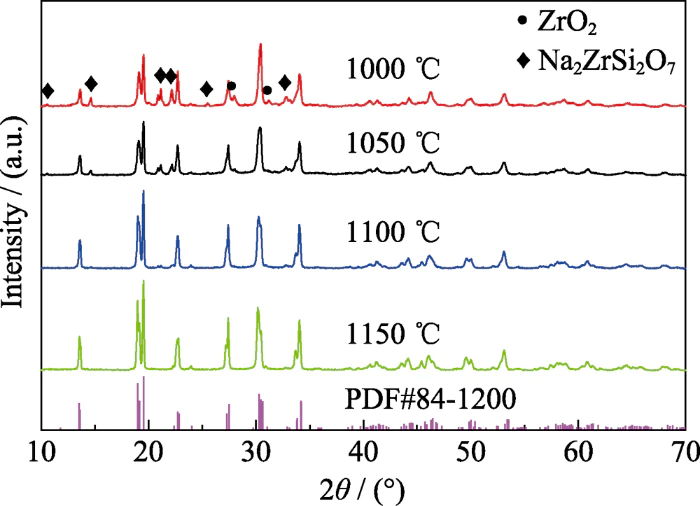
Fig. 1 DRX modèles de poudre Na3Zr2Si2PO12 frittée à différentes températures
La figure 2 montre des photos SEM et des photos TEM de Particules Na3Zr2Si2PO12 obtenues par mélange conventionnel et séchage par pulvérisation méthodes. La figure 2 (a) est une photo SEM de particules Na3Zr2Si2PO12 après mélange classique. On peut voir sur la photo que la forme du les particules sont irrégulières et le diamètre de certaines particules atteint 20 μm, indiquant que les particules après mélange conventionnel sont de grande taille et de forme inégale. La figure 2 (b ~ c) montre des photos SEM de particules Na3Zr2Si2PO12 après séchage par pulvérisation. Les particules sont sphériques et leur diamètre est moins de 5 μm, indiquant que la forme des particules est régulière et que la particule la distribution granulométrique est plus concentrée après séchage par pulvérisation. La figure 2 (d) est un TEM photo de la surface des particules Na3Zr2Si2PO12 après séchage par pulvérisation. Le la surface des particules est uniformément recouverte d'une couche de liant d'une épaisseur de environ 5 nm, ce qui favorise un contact plus étroit entre les particules céramiques.

Fig. 2 Images MEB de particules Na3Zr2Si2PO12 après traitement conventionnel mélange (a) et séchage par pulvérisation (b-c) et image TEM (d) de la surface des particules Na3Zr2Si2PO12 après pulvérisation séchage
La figure 3 montre la taille des particules diagramme de distribution du Na3Zr2Si2PO12 enrobé d'alcool polyvinylique (NZSP) obtenu par mélange conventionnel et le Na3Zr2Si2PO12 enrobé d'alcool polyvinylique (SD-NZSP) obtenu par la méthode de séchage par pulvérisation. On peut constater que le la largeur du demi-pic de la courbe de distribution granulométrique du SD-NZSP est plus étroite que celle de la courbe granulométrique NZSP, indiquant que la taille des particules la distribution après séchage par pulvérisation est plus concentrée. C'est fondamentalement cohérent avec les résultats présentés dans les photos SEM de la figure 2 (a, b). Dans De plus, la courbe de distribution granulométrique après séchage par pulvérisation est proche d'un répartition normale. Cette gradation granulométrique peut effectivement augmenter la contact entre les particules et réduire la porosité du corps vert. Comme indiqué dans le tableau 2, la densité du corps vert Na3Zr2Si2PO12 préparé par le La méthode de mélange conventionnelle est de 83,01 % et la densité du Na3Zr2Si2PO12 le corps vert préparé par le procédé de séchage par pulvérisation est augmenté à 89,12 %. En ordre pour explorer davantage l'effet de la taille des particules de Na3Zr2Si2PO12 sur la densité de la céramique et conductivité, balayage transversal, mesure de densité et des tests de conductivité ont été effectués sur des feuilles de céramique Na3Zr2Si2PO12 obtenues par méthodes conventionnelles de mélange et de séchage par pulvérisation.
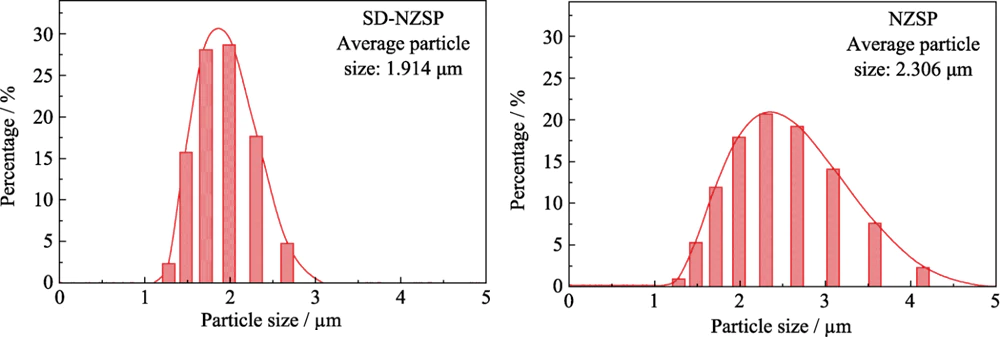
Fig. 3 Taille des particules Na3Zr2Si2PO12 profils de mélange conventionnel (NZSP) et de séchage par pulvérisation (SD-NZSP) mesurés par analyseur de particules laser
Tableau 2 Paramètres de frittage et paramètres de mesure de densité et résultats de mesure de l'électrolyte solide Na3Zr2Si2PO12 corps verts et feuille de céramique
|
Échantillon |
Température du processus/â |
Heure/h |
m/g |
réthanol/(g·cm-3) |
msubmergé/g |
rréel/(g·cm-3) |
rthéorique/(g·cm-3) |
rrelatif/% |
|
GB |
- |
- |
0,2902 |
0,785 |
0,2056 |
2,693 |
3,244 |
83.01 |
|
SD-GB |
- |
- |
0,2880 |
0.785 |
0,2098 |
2,891 |
3,244 |
89.12 |
|
CS-NZSP |
1250 |
6 |
0,2672 |
0,785 |
0,1938 |
2,858 |
3,244 |
88.10 |
|
SD-CS-NZSP |
1250 |
6 |
0,2644 |
0,785 |
0,1988 |
3,164 |
3,244 |
97,53 |
La figure 4 montre l'image physique du Feuille de céramique Na3Zr2Si2PO12, sa morphologie transversale et élémentaire diagramme d'analyse. La figure 4 (a) montre la morphologie en coupe transversale du pièce en céramique obtenue par la méthode de frittage classique. On a observé qu'il y avait de nombreux pores irréguliers dans la section transversale de la feuille de céramique, et le diamètre local des pores dépassait 5 μm. La raison est que la taille des particules après le broyage est inégal, il y a des particules plus grosses et il n'y a pas de proximité contact entre les particules, entraînant des pores plus irréguliers dans la céramique feuille pendant le processus de frittage secondaire. La figure 4 (b) montre le morphologie en coupe transversale de la pièce en céramique obtenue par séchage par pulvérisation méthode. Les grains de cristal sont en contact étroit les uns avec les autres et il y a pas de pores évidents. Cela montre que les particules Na3Zr2Si2PO12 de forme régulière et la distribution granulométrique concentrée peut facilement obtenir une haute densité feuilles de céramique pendant le processus de frittage secondaire. L'augmentation de la densité se reflète également dans l'augmentation du retrait du corps céramique après frittage, comme le montre la figure 4 (c). A gauche, une pièce en céramique obtenue par la méthode de frittage classique, avec un diamètre de 11,34 mm, et un retrait taux de seulement 5,5% ; à droite, une pièce en céramique obtenue par séchage par pulvérisation méthode, avec un diamètre de 10,36 mm, et un taux de retrait de 13,7 %. Pour explorer la composition de chaque élément de l'échantillon, une analyse élémentaire a été réalisée sur la section transversale de la pièce en céramique (Figure 4(b)), et Figure 4(d~g) a été obtenu. Le contenu de chaque élément est présenté dans le tableau 3. Chaque l'élément est réparti uniformément sur la section transversale de la pièce en céramique, et il n’y a pas d’agrégation d’éléments. D'après le tableau 3, on constate que Le pourcentage atomique de Na et P est de 2,98 : 1, ce qui est fondamentalement cohérent avec le formule chimique standard de Na:P=3:1, indiquant que l'excès de Na et de P dans le les matières premières peuvent compenser la volatilisation de Na et P pendant le processus de frittage.

Fig. 4 Images SEM de sections de tranches pour CS-NZSP (a) et SD-CS-NZSP (b), photographies correspondantes (c) et images de cartographie élémentaire (dg) de SD-CS-NZSP
Tableau 3 Analyse élémentaire d'une coupe de tranche de céramique Na3Zr2Si2PO12 par pulvérisation séchage/%
|
Élément |
O K |
Na K |
SiK |
PK |
ZrL |
|
Pourcentage atomique |
60.10 |
15.09 |
9,94 |
5.06 |
9,81 |
|
Pourcentage de poids |
36.43 |
13.13 |
10.59 |
5,94 |
33,91 |
2.2 Densité des feuilles de céramique Na3Zr2Si2PO12
L'expérience a mesuré la densité de Feuilles de céramique Na3Zr2Si2PO12 selon la méthode d'Archimède [30]. Afin d'étudier l'effet de la méthode de granulation sur la densité de la céramique Na3Zr2Si2PO12 Feuilles, dans les paramètres expérimentaux de préparation des feuilles de céramique, le paramètres expérimentaux (température de frittage, temps de maintien, etc.) du Le groupe expérimental témoin, à l’exception de la méthode de granulation, a été conservé le même. Dans afin de réduire l'impact des erreurs de mesures expérimentales sur la densité résultats, les mesures de densité ont été répétées sur les échantillons de feuilles de céramique obtenu par chaque méthode de préparation dans l’expérience. De l'expérimental données présentées dans le tableau 4, on peut voir que la densité de la céramique CS-NZSP feuilles obtenues par la méthode de frittage conventionnelle est de 88,1 %, ce qui correspond essentiellement cohérents avec les résultats rapportés dans la littérature [21]. La densité de Les feuilles de céramique SD-CS-NZSP obtenues par séchage par pulvérisation peuvent atteindre 97,5 %, ce qui est la valeur la plus élevée actuellement atteinte par les méthodes de frittage conventionnelles sans dopage des éléments. Elle est encore plus élevée que la densité de la céramique Na3Zr2Si2PO12 tôles obtenues par d'autres méthodes de frittage rapportées dans la littérature. Tel que méthode de frittage par micro-ondes (96 %) [23], méthode de frittage à froid (93 %) [24], méthode de frittage liquide méthode de frittage en phase (93 %) [26] et méthode de frittage par plasma de décharge (97,0 %) [29].
Tableau 4 Conductivité ionique du CS-NZSP et SD-CS-NZSP à température ambiante
|
Échantillon |
sb/(S·cm-1) |
sgb/(S·cm-1) |
st/(S·cm-1) |
Ea/eV |
|
CS-NZSP |
1.28Ã10-3 |
8.03Ã10-4 |
4.94Ã10-4 |
0,34 |
|
SD-CS-NZSP |
1.64Ã10-3 |
1.21Ã10-3 |
6.96Ã10-4 |
0,32 |
2.3 Performances électriques Na3Zr2Si2PO12 tester
La figure 5 (a) montre la température ambiante spectre d'impédance électrochimique (EIS) de la plaquette de céramique obtenue par méthode de frittage conventionnelle et méthode de séchage par pulvérisation. Le demi-cercle dans le la figure reflète les caractéristiques d'impédance parallèle du joint de grain impédance et réactance capacitive. L'intersection entre le côté gauche de le demi-cercle et l'abscisse représentent la résistance du grain. Le l'envergure du demi-cercle en abscisse reflète la résistance du grain limite, et la ligne oblique après le demi-cercle reflète l'impédance caractéristiques de l’interface électrode de blocage/électrolyte [36]. Par en ajustant l'EIS sur la figure 4, la conductivité ionique de CS-NZSP et SD-CS-NZSP peut être obtenu. Les données expérimentales sont présentées dans le tableau 4. La salle conductivité ionique en température du SD-CS-NZSP obtenue par séchage par pulvérisation La méthode est de 6,96 × 10-4 S × cm-1, ce qui est supérieur à celui du CS-NZSP (4.94Ã10-4 Sâcm-1) obtenu par la méthode de frittage conventionnelle. À travers le analyse des données de l'ajustement EIS, on peut voir que SD-CS-NZSP avec un la densité a une résistance aux joints de grains plus petite et une température ionique plus élevée conductivité.
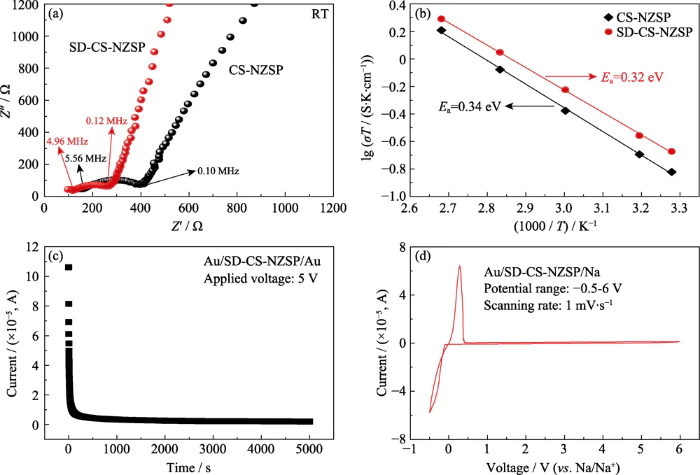
Fig. 5 (a) spectres EIS à température ambiante et (b) Courbes d'Arrhenius de CS-NZSP et SD-CS-NZSP ; (c) Polarisation potentiostatique CC courant et (d) fenêtre électrochimique pour SD-CS-NZSP
La figure 5(b) montre les courbes d'Arrhenius de température ambiante jusqu'à 100°C pour les feuilles de céramique obtenues par différentes préparations méthodes. On peut voir sur la figure que leur conductivité augmente avec température croissante. Lorsque la température atteint 100 °C, la conductivité de SD-CS-NZSP peut atteindre 5,24 × 10-3 Sâcm-1, soit un ordre de magnitude supérieure à la conductivité à température ambiante. Son énergie d'activation est ajusté selon l'équation d'ArrheniusÏ=Aexp(-Ea/kT)[7]. Les énergies d'activation de CS-NZSP et SD-CS-NZSP ont été obtenus respectivement à 0,34 et 0,32 eV, ce qui sont similaires au rapport de YANG et al. [18].
Les matériaux électrolytiques solides doivent avoir à la fois une conductivité ionique élevée et une faible conductivité électronique. Par conséquent, le La conductivité électronique du SD-CS-NZSP a été mesurée par courant continu polarisation (DC), et la courbe de polarisation correspondante est représentée sur la figure 5(c). On peut voir sur la figure qu'à mesure que la durée du test se prolonge, le le courant de polarisation diminue progressivement ; lorsque le temps de test atteint 5000 s, le courant de polarisation (I = 3,1 μA) ne change plus avec la durée du test prolonge. Calculée à l'aide des formules (2, 3), la conductivité électronique de SD-CS-NZSP est de 1,23 × 10-7 S × cm-1 et l'ion sodium le numéro de migration est 0,9998. L'étude a également mesuré la fenêtre électrochimique de SD-CS-NZSP par voltamétrie cyclique (CV) [18]. Comme le montre la figure 5(d), deux des pics d'oxydation et de réduction apparaissent vers 0 V, représentant le décapage et dépôt de sodium respectivement [20]. A part ça, aucun autre redox des pics ont été observés dans la plage de tension balayée. Cela signifie qu'il y a aucun changement de courant dû à la décomposition de l'électrolyte dans la tension plage de 0 ~ 6 V, indiquant que le SD-CS-NZSP a une bonne stabilité électrochimique. La large fenêtre électrochimique (6 V (vs Na/Na+)) peut correspondre à l'ion sodium électrolyte solide aux matériaux cathodiques haute tension, tels que Matériaux cathodiques à base de nickel-manganèse, ce qui est bénéfique pour améliorer la densité énergétique des batteries sodium-ion.
3 Conclusion
Une méthode en phase solide à haute température a été utilisé pour synthétiser de la poudre Na3Zr2Si2PO12 en phase pure à une température de frittage de 1150°C en introduisant un excès de Na et de P dans le précurseur. Utilisation du séchage par pulvérisation pour granuler la poudre de manière sphérique, le liant alcool polyvinylique est uniformément enduit sur la surface des particules de Na3Zr2Si2PO12 et la taille des particules la distribution est proche de la distribution normale. La densité du préparé La céramique Na3Zr2Si2PO12 atteint 97,5 %. Une densité accrue peut réduire efficacement résistance aux limites des grains et la conductivité ionique atteint 6,96 × 10-4 S × cm-1 à température ambiante, ce qui est supérieur à celui des feuilles de céramique préparé par des méthodes de frittage conventionnelles (4,94 × 10-4 Sâcm-1). De plus, le les céramiques produites par la méthode de séchage par pulvérisation ont une large fenêtre électrochimique (6 V (vs Na/Na+)) et peut être associé à des matériaux cathodiques haute tension pour augmenter la densité énergétique de la batterie. On peut voir que le spray la méthode de séchage est une méthode efficace pour préparer des électrolytes céramiques Na3Zr2Si2PO12 avec une densité élevée et une conductivité ionique élevée, et convient à d'autres types d'électrolytes solides céramiques.
Références
[1] JIAN Z L, ZHAO L, PAN H L, et al. Na3V2(PO4)3 recouvert de carbone comme nouveau matériau d'électrode pour les batteries sodium-ion. Communications électrochimiques, 2012,14(1):86-89.
[2] ZHAO L, ZHAO J M, HU Y S, et al. Téréphtalate disodique (Na2C8H4O4) comme matériau d'anode haute performance pour batterie sodium-ion à faible coût à température ambiante. Matériaux énergétiques avancés, 2012,2(8):962-965.
[3] RUAN Y L, GUO F, LIU J J, et al. Optimisation de l'électrolyte céramique Na3Zr2Si2PO12 et de l'interface pour des performances élevées batterie au sodium à semi-conducteurs performante. Céramique Internationale, 2019,45(2):1770-1776.
[4] VETTER J, NOVAK P, WAGNER MR, et al. Mécanismes de vieillissement des batteries lithium-ion. Journal des sources d'énergie, 2005,147(1/2):269-281.
[5] KAMAYA N, HOMMA K, YAMAKAWA Y, et al. UN conducteur superionique au lithium. Matériaux naturels, 2011,10(9):682-686.
[6] TARASCON J M, ARMAND M. Enjeux et défis auxquels sont confrontées les batteries au lithium rechargeables. Nature, 2001,414(6861):359-367.
[7] KHOKHAR W A, ZHAO N, HUANG W L, et al. Différents comportements de pénétration des métaux dans les électrolytes solides Na et Li. ACS Matériaux appliqués et interfaces, 12(48):53781-53787.
[8] OUDENHOVEN JF M, BAGGETTO L, NOTTEN P H L. Microbatteries lithium-ion entièrement solides : un examen de diverses notions dimensionnelles. Matériaux énergétiques avancés, 2011,1(1):10-33.
[9] ZHAO C L, LIU L L, QI X G, et al. Piles au sodium à semi-conducteurs. Matériaux énergétiques avancés, 2017,8(17):1703012.
[10] HAYASHI A, NOI K, SAKUDA A, et al. Électrolytes vitrocéramiques superioniques pour sodium rechargeable à température ambiante piles. Nature Communications, 2012,3:856.
[11] LOU S F, ZHANG F, FU C K, et al. Problèmes et défis d'interface dans les batteries tout solide : lithium, sodium, et au-delà. Matériaux avancés, 2020,33(6):2000721.
[12] HUANG W L, ZHAO N, BI Z J et al. Peut trouvons-nous une solution pour éliminer la pénétration du Li à travers les électrolytes solides du grenat ? Matériaux aujourd'hui Nano, 2020,10:100075.
[13] JIAN Z L, HU Y S, JI XL, et al. Matériaux structurés NASICON pour le stockage d'énergie. Matériaux avancés, 2016,29(20):1601925.
[14] HOU W R, GUO X W, SHEN X Y, et al. Électrolytes solides et interfaces dans les batteries au sodium tout solide : progrès et le point de vue. Nano Énergie, 2018,52 :279-291.
[15] GOODENOUGH JB, HONG H Y P, KAFALAS J A. Transport rapide des ions Na+ dans les structures squelettiques. Bulletin de recherche sur les matériaux, 1976,11(2):203-220.
[16] HONG H Y P. Structures cristallines et chimie cristalline dans le système Na1+xZr2SixP3-xO12. Recherche sur les matériaux Bulletin, 1976,11(2):173-182.
[17] RAN LB, BAKTASH A, LI M, et al. Sc, Le co-dopage Ge NASICON améliore les performances des batteries sodium-ion à semi-conducteurs. Matériaux de stockage d'énergie, 2021,40:282-291.
[18] YANG J, LIU G Z, AVDEEV M, et al. Piles rechargeables ultrastables au sodium entièrement solides. Lettres énergétiques ACS, 2020,5(9):2835-2841.
[19] LENG H Y, HUANG J J, NIE J Y, et al. Frittage à froid et conductivités ioniques du solide Na3.256Mg0.128Zr1.872Si2PO12 électrolytes. Journal des sources d'énergie, 2018, 391 : 170-179.
[20] HUANG C C, YANG G M, YU W H, et al. Électrolytes solides Nasicon Na3Zr2Si2PO12 substitués au gallium. Journal des alliages Et Composés, 2021,855:157501.
[21] ZHANG Z Z, ZHANG Q H, SHI J N, et al. Électrolyte composite autoformant pour batterie au sodium à l'état solide avec durée de vie ultra longue. Matériaux énergétiques avancés, 2017,7(4):1601196.
[22] ANANTHARAMULU N, RAO K K, RAMBABU G, et coll. Une revue approfondie des matériaux de type Nasicon. Journal des matériaux Science, 2011,46(9):2821-2837.
[23] WANG X X, LIU Z H, TANG Y H, et al. Frittage à basse température et rapide par micro-ondes du solide Na3Zr2Si2PO12 électrolytes pour batteries Na-ion. Journal des sources d'énergie, 2021,481:228924.
[24] GRADY Z M, TSUJI K, NDAYISHIMIYE A, et al. Densification d'un électrolyte sodium-ion NASICON à l'état solide en dessous de 400 â par frittage à froid avec un solvant hydroxyde fondu. Matériaux énergétiques appliqués ACS, 2020,3(5):4356-4366.
[25] SHAO Y J, ZHONG G M, LU Y X, et al. UN nouvel électrolyte composite vitrocéramique à base de NASICON avec ions Na améliorés conductivité. Matériaux de stockage d'énergie, 2019,23:514-521.
[26] LENG H Y, NIE J Y, LUO J. Combinant frittage à froid et frittage en phase liquide activé par Bi2O3 pour fabriquer NASICON dopé au magnésium à haute conductivité à des températures réduites. Journal de Matériomique, 2019,5(2):237-246.
[27] OH JAS, HELC, PLEWA A et al. Électrolyte solide composite NASICON (Na3Zr2Si2PO12) avec Na+ amélioré conductivité ionique : effet du frittage en phase liquide. Matériaux appliqués ACS &Interfaces, 2019,11(43):40125-40133.
[28] DA SILVA JGP, BRAM M, LAPTEV A M, et al. Frittage d'un électrolyte NASICON à base de sodium : une étude comparative entre les méthodes de frittage à froid, assistées sur site et conventionnelles. Journal de la Société européenne de la céramique, 2019,39(8):2697-2702.
[29] WANG H, OKUBO K, INADA M, et al. Faible céramiques à base de NASICON densifiées en température favorisées par le verre Na2O-Nb2O5-P2O5 frittage additif et plasma par étincelle. Solid State Ionics, 2018, 322 : 54-60.
[30] HUO HY, GAO J, ZHAO N, et al. UN bouclier interfacial flexible bloquant les électrons pour le lithium solide sans dendrites piles métalliques. Nature Communications, 2021,12(1):176.
[31] JIA MY, ZHAO N, HUO HY, et al. Enquête approfondie sur les électrolytes du grenat vers batteries au lithium solides orientées applications. Avis sur l'énergie électrochimique, 2020,3(4):656-689.
[32] ZHAO N, KHOKHAR W, BI Z J, et al. Piles en grenat solide. Joule, 2019,3(5):1190-1199.
[33] VERTRUYEN B, ESHRAGHI N, PIFFET C, et al. Séchage par pulvérisation de matériaux d'électrodes pour batteries lithium-ion et sodium-ion. Matériaux, 2018,11(7):1076.
[34] KOU Z Y, MIAO C, WANG Z Y, et al. Nouveau solide structurel Li1.3Al0.3Ti1.7SixP5(3-0.8x)O12 de type NASICON électrolytes à conductivité ionique améliorée pour batteries lithium-ion. Solide State Ionics, 2019,343:115090.
[35] SHEN L, YANG J, LIU G Z, et al. Haut conductivité ionique et électrolyte solide NASICON résistant aux dendrites pour piles au sodium entièrement solides. Matériaux aujourd'hui Énergie, 2021,20:100691.
[36] LI Y Q, WANG Z, LI C L, et al. Densification et amélioration de la conduction ionique du solide de grenat de lithium électrolytes par frittage d'oxygène circulant. Journal des sources d'énergie, 2014,248 :642-646.



